Azotlu asit
| Azotlu asit | |
 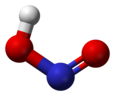  Cis ve trans nitröz asidin yapısı . |
|
| Kimlik | |
|---|---|
| IUPAC adı |
azotlu asit hidrojen nitrit |
| N O CAS | |
| K O AKA | 100.029.057 |
| N O EC | 231-963-7 |
| PubChem | 24529 |
| chebi | 25567 |
| gülümser |
N (= O) O , |
| InChI |
InChI: InChI = 1S / HNO2 / c2-1-3 / h (H, 2,3) InChIKey: IOVCWXUNBOPUCH-UHFFFAOYSA-N |
| Görünüm | soluk mavi çözüm |
| Kimyasal özellikler | |
| formül |
H N O 2 [İzomerler] |
| Molar kütle | 47.0134 ± 0.0009 g / mol H %2.14, N %29.79, O %68.06, |
| pKa | 25 ° C'de 3,35 |
| dipolar moment |
1.423 ± 0.005 D ( cis ) 1.855 ± 0.016 D ( trans ) |
| elektronik özellikler | |
| 1 yeniden iyonlaşma enerjisi | ≤ 11,3 eV (gaz) |
| Aksi belirtilmedikçe SI ve STP birimleri . | |
Nitröz asit a, kimyasal bileşik arasında formül HNO 2. Sadece çok asidik olmayan bir çözeltide (düşük pH'ta dağılır) ve gaz fazında bilinen zayıf bir mono asittir . Tuzları ( nitritler ) sulu çözeltide stabildir. Azotlu asit, azo boyaların hazırlanmasında temel reaktiflerden biridir. Daha sonra düşük sıcaklıkta (yaklaşık 5 °C) sodyum nitritin asitleştirilmesiyle yerinde hazırlanır .
HNO 2 molekülüIRAS 16293−2422 (tr) ikili sisteminin B bileşenindeki yıldızlararası ortamda tespit edildi .
Açıklama
Sistematik adı: dioksonitrik asit (III) veya nitrik asit III'tür . Tuzlarına nitrit denir .
Özellikle kararsızdır ve oda sıcaklığında nitrojen monoksit NO ve nitrat iyonuna [NO 3 ] dönüşür -Ve Şekil Frost diyagramı ait azot , aşağıda verilen:

+ III oksidasyon durumunda olan azot, orantısızlaştırmadan sonra + V ve + II hallerinde bulunur.
Azo türevlerini hazırlamak için nitröz asit kullanılır ( azobenzen C 6 H 5 –N = N – C 6 H 5) aromatik aminlerden , diazonyum tuzları yoluyla C 6 H 5 –N + ≡N · X -.
Onun pKa bir 3.3 olduğunu.
İlave depolanacak çok kararsız olduğu için, doğaçlama olarak hazırlanmaktadır hidroklorik asit ile sodyum nitrit çözeltisi içinde:
NO 2 - (sulu)+ H 3 O +→ HNO2 (sulu)+ H 2 O (sıvı).Şuna da bakın:
Notlar ve referanslar
- (içinde) David R. Lide, Handbook of Chemistry and Physics , CRC,16 Haziran 2008, 89 inci baskı. , 2736 s. ( ISBN 142006679X ve 978-1420066791 ) , s. 9-50
- hesaplanan moleküler kütlesi " Elements 2007 Atom ağırlıkları " üzerine www.chem.qmul.ac.uk .
- (içinde) David R. Lide, Handbook of Chemistry and Physics , CRC,2008, 89 inci baskı. , 2736 s. ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- (içinde) A. Coutens, NFW Ligterink, BC Loison, V. Wakelam, H. Calcutt, MN Drozdovskaya JK Jørgensen, HSP Müller, EF van Dishoeck ve SF Wampfler , " ALMA PILS araştırması: Nitröz asidin ilk tespiti (HONO) ) yıldızlararası ortamda ” , Astronomy & Astrophysics , cilt. 623, Mart 2019, Makale n o L13 ( DOI 10,1051 / 201935040 / 0004-6361 , bibcode 2019A & A ... 623L..13C , arXiv 1903,03378 , çevrimiçi okuma )