Florosülfürik asit
| Florosülfürik asit | |
 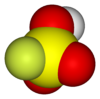 Florosülfürik asidin yapısı. |
|
| Kimlik | |
|---|---|
| IUPAC adı | florosülfürik asit |
| Eş anlamlı |
florosülfonik asit |
| N O CAS | |
| K O AKA | 100.029.227 |
| N o EC | 232-149-4 |
| N O RTECS | LP0715000 |
| PubChem | 24603 |
| GÜLÜMSEME |
OS (= O) (= O) F , |
| InChI |
InChI: InChI = 1S / FHO3S / c1-5 (2,3) 4 / h (H, 2,3,4) InChIKey: UQSQSQZYBQSBJZ-UHFFFAOYSA-N |
| Görünüm | renksiz sıvı |
| Kimyasal özellikler | |
| Kaba formül | HSO 3 Fveya HFSO 3 |
| Molar kütle | 100,07 ± 0,006 g / mol H% 1,01, F% 18,99, O% 47,96, S% 32,04, |
| pKa | -10 |
| Fiziki ozellikleri | |
| T ° füzyon | -87.3 ° C |
| T ° kaynama | 165.5 ° C |
| Çözünürlük | Suda çözünür |
| Hacimsel kütle | 1.84 (sıvı) |
| Önlemler | |
| SGH | |
  Tehlike H314, H332, H314 : Ciddi cilt yanıklarına ve göz hasarına neden olur H332 : Solunması halinde zararlıdır. |
|
| WHMIS | |
  E, F, E : Aşındırıcı malzeme Tehlikeli malların taşınması: sınıf 8 F : Tehlikeli reaktif madde suyla temas ettiğinde şiddetli reaksiyona girer ve çok zehirli bir gaz açığa çıkarır: hidrojen klorür İçerik açıklama listesine göre% 1,0 oranında açıklama |
|
| Aksi belirtilmedikçe SI ve STP birimleri . | |
Fluorosulfuric asit olarak da adlandırılan, asit fluorosülfonik , a, kimyasal bileşik arasında , formül HSO 3 F. Bu bir düşük viskoziteli bir sıvı içinde çözünür, polar çözücüler gibi nitrobenzen , asetik asit ve etil asetat , ancak bu tür polar olmayan çözücüler içinde zayıf çözünürlüğe sahip alkanlar . Antimon pentaflorür SbF 5 ile eş molar karışımı olan -10'a eşit bir pK a süperasiti .verir sihirli asit HSO 3 F SbF 5Bir güçlü bir asit da bilinir. Bu asitlik, zayıf proton alıcı bileşikler dahil hemen hemen her organik maddeyi çözmesine izin verir.
HSO 3 Fs' hidroliz yavaşça hidroflorik asit ve sülfürik asit ; Triflik asit HSO 3 CF 3Yapısal olarak buna bağlı olan, suda daha kararlıdır.
Özellikleri
Florosülfürik asit, bir -OH grubunun bir flor atomu ile değiştirildiği bir sülfürik asit molekülü olarak görülebilir . Elektronegatiflik oksijen, elde edilen ürünün asit bir artışa yol açar daha büyük olan flor,.
Hazırlık
Florosülfürik asit, hidrojen florür HF'nin sülfür trioksit SO 3 ile reaksiyona sokulmasıyla hazırlanır. :
SO 3+ HF → HSO 3 F.Devam etmenin bir başka yolu da potasyum biflorür KHF 2'ye saldırmaktır.veya kalsiyum florür CaF 2oleum tarafından H 2 S 2 O 7en 250 ° C , sonra distile olur HSO için 3 FNadir bir gazın sirkülasyonu ile hidrojen florürün buradan uzaklaştırılmasından sonra .
kullanım
Florosülfürik asit, HF ve H 2 SO 4 karışımlarını üretmek için kullanılır.için işlemek kristal . Bu teşvik izomerizasyonunu arasında alkanlar ve alkilasyon arasında hidrokarbonlar ile alkenler henüz bu reaksiyon ve teknik açıdan ilginç olabilir olup olmadığı bilinmemektedir, ancak. Laboratuvarda florlama ajanı olarak da kullanılabilir.
Notlar ve referanslar
- hesaplanan moleküler kütlesi " Elements 2007 Atom ağırlıkları " üzerine www.chem.qmul.ac.uk .
- 1272/2008 (16 Aralık 2008) AT yönetmeliği Ek VI tablo 3.1'deki dizin numarası
- " florosülfonik asit kimyasalları veritabanında" Reptox ait CSST 25 Nisan 2009 erişilen (iş güvenliği ve sağlığı sorumlu Quebec örgütü),