Hidrojen florid
| Hidrojen florid | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Hidrojen florür molekülü |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kimlik | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC adı |
hidroflorik asit Hidrojen florür |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| K O AKA | 100.028.759 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 231-634-8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Görünüm | Keskin bir kokuya sahip renksiz gaz veya renksiz sıvı. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kimyasal özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kaba formül |
H F [İzomerler] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar kütle | 20.00634 ± 0 g / mol H% 5.04, F% 94.96, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipolar moment | 1.826178 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moleküler çap | 0.290 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fiziki ozellikleri | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° füzyon | -83 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kaynama | 20 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Çözünürlük | suda: çok iyi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Çözünürlük parametresi δ | 33.0 J 1/2 · cm -3/2 (≤ 20 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
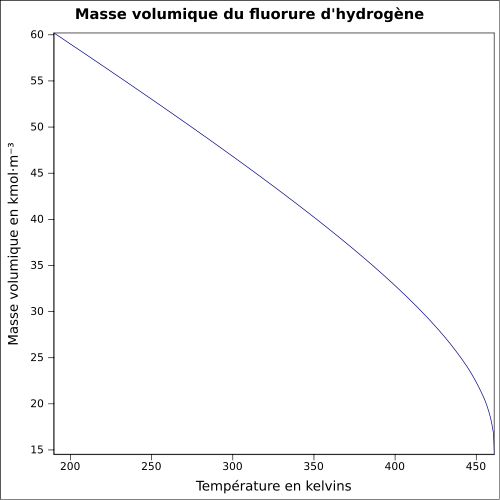
| Hacimsel kütle |
1,0 g · cm -3
denklem:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kendiliğinden tutuşma sıcaklığı | yanıcı değil | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doygun buhar basıncı | de 25 ° C : 122 kPa
denklem:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritik nokta | 64,8 bar , 187,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termokimya | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 gaz, 1 bar | 173.7 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gaz | - 271,1 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 sıvı | - 299,8 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 4.6 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ buhar H ° | 7,5 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
51,7 J · K -1 · mol -1 (sıvı) 29,1 J · K -1 · mol -1 (gaz)
denklem:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronik özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re iyonlaşma enerjisi | 16.044 ± 0.003 eV (gaz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optik özellikler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kırılma indisi | 1.340 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Önlemler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Tehlike H300, H310, H314, H330, H300 : Yutulması halinde öldürücüdür H310 : Cilt ile temasında öldürücüdür H314 : Ciddi cilt yanıklarına ve göz hasarına neden olur H330 : Solunması halinde öldürücüdür |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  D1A, D2A, E, D1A : Ciddi ani etkilere neden olan çok toksik malzeme Akut ölüm: LC50 soluma / 4 saat (fare) = 171 ppm D2A : Diğer toksik etkilere neden olan çok toksik malzeme Kronik toksisite: Floroz E : Aşındırıcı malzeme Tehlikeli malların taşınması: sınıf 8 Açıklama içerik açıklama listesine göre% |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 0 4 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ulaşım | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
886 : çok aşındırıcı ve toksik malzeme UN numarası : 1052 : SUSUZ HİDROJEN FLORÜR Sınıfı: 8 Sınıflandırma kodu: CT1 : Zehirli aşındırıcı maddeler: Sıvılar; Etiketler: 8 : Aşındırıcı maddeler 6.1 : Zehirli maddeler Ambalaj: Paketleme grubu I : çok tehlikeli maddeler;   |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soluma | Çok toksik | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cilt | Çok aşındırıcı, Çok toksik | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gözler | Çok aşındırıcı | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Yutma | Çok toksik | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoksikoloji | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Koku eşiği | düşük: 0,04 ppm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aksi belirtilmedikçe SI ve STP birimleri . | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hidrojen florür , renksiz bir kimyasal formül HF'dir (atomudur , hidrojen (H) atomu ve bir florin (F)). Keskin bir kokusu vardır, çok aşındırıcıdır ve çok kolay sıvılaşır.
Teorik olarak, hidrojen florür sıvılaştırılması zor bir gaz olmalıdır, ancak oda sıcaklığında sıvı haldedir. Bu anormallik, hidrojen florürün dimerize formda (HF) 2 mevcut olmasından kaynaklanmaktadır .
Kimya
HF hidrojen florür molekülü, tek bir bağ ile bağlanmış bir hidrojen atomu H ve bir flor atomu F'den oluşan diatomik bir moleküldür . Flor, hidrojenden çok daha elektronegatif olduğu için bağ çok polarize olmuştur. Sonuç olarak molekül , flor atomu tarafından taşınan negatif kısmi yük δ- ve hidrojen atomu tarafından taşınan pozitif kısmi yük δ + ile büyük bir dipol momenti taşır . Hidrojen florür bu nedenle polar bir moleküldür. Suda ve polar çözücülerde çok çözünür. Hidrojen florürün suda çözünmesi şiddetli bir ekzotermik reaksiyondur ve sıçrama meydana gelebileceğinden dikkatle yürütülmesi gerekir.
Sulu çözeltide, hidrojen florür , seyreltik çözeltide zayıf asit, ancak konsantre çözelti içinde güçlü olan hidroflorik asit oluşturur .
Hazırlık
Hidrojen florür, sülfürik asit ile karıştırılmış kalsiyum florürden sentezlenir .
CaF 2 + H 2 SO 4 → CaSO 4 + 2 HFBu reaksiyonla elde edilen buharlar, küçük miktarlarda hidrojen florür, sülfürik asit ve diğer ürünlerin bir karışımıdır. Hidrojen florür, damıtma yoluyla izole edilebilir .
Ayrıca, ara ürün olarak hipoflor asit ile suyun diflorür ile oksidasyonu ile sentezlenebilir . Son derece kararsız olan ikincisi, patlayıcı bir şekilde kendiliğinden hidrojen florür ve oksijene ayrışır .
kullanım
Hidrojen florür, farmasötikler ve polimerler ( Teflon ) gibi birçok bileşiğin sentezinde önemli bir öncüdür . Hidrojen florür ayrıca petrol endüstrisinde ve süperasitlerin bileşiminde yaygın olarak kullanılmaktadır .
Hidrojen florür, mikroelektronik işlemlerde çok yaygın olarak kullanılmaktadır . Özellikle silikon dioksit tabakalarını çıkarmak için kullanılır .
Hidrojen florür de dönüştürmek için, nükleer sanayide katılır uranyum dioksit içine uranyum tetraflorürün , üretiminde bir ara ürün uranyum hegzaflorid . İkinci element, uranyum zenginleştirmesinin bir girdi ürünüdür .
güvenlik
Hidrojen florür yanıcı olmayan bir gazdır, ancak nem varlığında çoğu metalle reaksiyona girerek çok yanıcı bir gaz olan hidrojeni oluşturur . Alkalilerle reaksiyon çok şiddetli olabilir.
Hidrojen florür havadan daha ağır bir gazdır ve yer altında veya dar alanlarda birikebilir. Risklerden kaçınmak için havalandırılan bir yerde saklanmalıdır. Nemli bir atmosferde beyaz buharlar çıkarır. Florür iyonlarının aşırı emilmesi akut floroza neden olabilir .
Ayrıca oluşturmak üzere su ile reaksiyona girer , hidroflorik asit , bir çok aşındırıcı asit . Suyun pH'ını değiştirdiği için bu ürün çevreye salınmamalıdır .
Dış bağlantılar
Ayrıca görün
Referanslar
- HYDROGEN FLUORIDE , Uluslararası Kimyasal Güvenlik Programının güvenlik sayfaları , 9 Mayıs 2009 tarihinde başvurulmuştur.
- (inç) David R. Lide, Kimya ve Fizik El Kitabı , CRC,16 Haziran 2008, 89 inci baskı. , 2736 s. ( ISBN 978-1420066791 ) , s. 9-50
- (en) Yitzhak Marcus, Çözücülerin Özellikleri , cilt. 4, İngiltere, John Wiley & Sons Ltd,1999, 239 s. ( ISBN 0-471-98369-1 )
- hesaplanan moleküler kütlesi " Elements 2007 Atom ağırlıkları " üzerine www.chem.qmul.ac.uk .
- (en) Robert H. Perry ve Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 inci baskı. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- " Properties of Various Gases " , flexwareinc.com ( 12 Nisan 2010'da erişildi )
- Genel ve mineral kimyasının olağan - M.Bernard - F.Busnot - Dunod - 1984
- (inç) David R. Lide, Kimya ve Fizik El Kitabı , Boca Raton, CRC,2008, 89 inci baskı. , 2736 s. ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- "Hydrogen fluoride" , ESIS'te , erişim tarihi 11 Şubat 2009
- IFA'nın (mesleki güvenlik ve sağlıktan sorumlu Alman kuruluşu) GESTIS kimyasal veritabanına "7664-39-3" CAS numarası girişi ( Almanca , İngilizce ), 27 Kasım 2008'de erişildi (JavaScript gerekli)
- 1272/2008 (16 Aralık 2008) AT yönetmeliği Ek VI tablo 3.1'deki endeks numarası
- " Hidrojen florür kimyasal ürünlerin veritabanındaki" Reptox ait CSST 25 Nisan 2009 erişilen (iş güvenliği ve sağlığı sorumlu Quebec örgütü),
- " Hydrogen fluoride " , hazmap.nlm.nih.gov'da (erişim tarihi 14 Kasım 2009 )
- Areva - Doğal uranyumun dönüşümü