Organomagnezyum
Bir organomagnezyum bir bir organik bileşik , bir ile karbon - magnezyum bağı . Bu önemli bir aile olan organometalik bileşikler olarak organik sentez içerdiği için Grignard'ın reaktif bir şekilde karıştırılmış organomagnesiums olan, R - Mg X , Ra, bir karbon zinciri ve X, a, halojen , genel olarak brom. Ya da klor , bazen, iyot - florin , genel olarak çok düşük dolayı kullanılmaz polarize ait difluor F 2. Bu reaktifler endüstride yaygın olarak kullanılan ve geç onların keşif XIX inci Fransız kimyager tarafından yüzyılın Victor Grignard almak almasına olanak sağladı kimya dalında Nobel Ödülü onlar çünkü 1912 yılında bağlanan çeşitli yapı taşları arasında hiç moleküllerin organik.
Grignard reaktifleri ilave olarak, organomagnezyum bileşikleri, örneğin moleküller bulunmaktadır dimethylmagnesium (CH 3 ) 2 , Mg, Dibütilmagnezyum (CH 3 CH 2 CH 2 CH 2 ) 2 , Mgveya antrasen-magnezyum .
R - Mg - X'in organometalik karakteri
Karbon bir sahiptir elektronegatiflik güçlü: . Ve bunu da fark ediyoruz . C: M - Bu fiziksel olgu dolayısıyla C kutuplaşmayı getirir -M bağlantısını . Klasik karbon bağlarının kutupluluğunun tersine döndüğünü fark ediyoruz : bir organometalikte karbon bir yük taşır (bu karbon karbanyon olarak adlandırılır), ayrıca bu bağ% 35 iyoniktir ve bu, örneğin bir halojen alkil ( R — X ) bir karbondan karbona bağı oluşturur .
Organomagnezyumlar, 40 ila 60 arasında bir pKa ile organik kimyadaki en güçlü Brönsted bazlarından biridir. R-Mg-X, güçlü bir nükleofildir .
Organomagnezyum sentezi
Aşırı bazikliklerinden dolayı, organomagnezyum doğal olarak mevcut değildir. Sentezin genel sonuçları aşağıdaki gibidir:
Çalışma modu
Sentez organomagnezyumun hassas: Reaksiyon ortamı , arzu edilen ürünün özellikleri, susuz olması gerekir; reaksiyon güçlü bir şekilde ekzotermiktir ve çözücü uçucu ve yanıcıdır. Yanlış kullanım aynı zamanda " Wurtz Bağlantısı " adı verilen parazitik bir ürünün oluşmasına da neden olur .
Gerekli malzemeler :
- Üç renkli top;
- İzobarik döküm hunisi;
- Geri akış yoğunlaştırıcı;
- CaCl 2'yi tutar (veya inert bir atmosfer altında çalışır);
- Isıtmalı manyetik karıştırıcı;
- Magnezyum talaşı;
- Dietil eter veya susuz THF;
- Halojenlenmiş türev;
- Su banyosu ve ardından soğuk su.
Çalışma modu
- Reaksiyon ortamını atmosferik neme karşı koruyarak ve üç boyunlu şişeye oval bir manyetik çubuk yerleştirerek geri akışlı bir ekleme düzeneği gerçekleştirin.
- Daha önce fırında etkinleştirilmiş magnezyum talaşlarını trikole yerleştirin. Üzerlerini birkaç cm 3 susuz etil eterle örtün . Küçük bir diyot kristali ekleyin.
- Dökme hunisini susuz etil eter içindeki halojenlenmiş türevin çözeltisiyle koşullandırın ve bir cam tıpa ile kapatın.
- Magnezyum talaşı üzerine birkaç damla halojenür solüsyonu dökün, reaksiyon ortamında meydana gelen bir renk değişikliğinin gözlemlenmesi için birkaç dakika bekleyin.
- Reaksiyon ortamında iyotun rengi kaybolduğunda, bir geri akış oluşturmak için bir su banyosunda ısıtın ve manyetik olarak karıştırarak halidi yavaşça ve damla damla dökün.
- Ekleme tamamlandıktan sonra, tam bir reaksiyon elde etmek için reaksiyon ortamını geri akışa ısıtın.
Yorumlar (değiştir | kaynağı değiştir)
Sentezlenen organomagnezyum ve halojenür arasında bir Würtz eşleşmesinin oluşmasını önlemek için . Reaksiyonun başlangıcından itibaren eter kaynar: geri akış, şişede akan eter buharlarını yoğunlaştırmaya yarar; yukarıda bahsedilen parazitik reaksiyonu yaratmamak için geri akış da çok düşük tutulmalıdır. Manipülasyon boyunca ısıtmaya gerek yoktur çünkü reaksiyon çok ekzotermiktir .
Nihai olarak elde edilen çözelti genel olarak oldukça açık grimsi bir renktedir.
Çözücü
Eter burada çift rol oynar, oluşan organomagnezyumu çözer ve onu stabilize eder, organomagnezyum burada bir Lewis asididir, buradaki çözücü Lewis bazının rolünü oynar , bu nedenle bağlayıcı olmayan oksijen çiftleri , reaktif merkezini stabilize etmeye gider. magnezyum . Örneğin dietil eter veya THF - tetrahidrofuran kullanmak mümkündür , bkz. Aşağıdaki şekil.

Organomagnezyumun yıkandığı ortam tamamen susuz olmalıdır : su / RMgX reaksiyonu canlıdır.
Organomagnezyumun reaktivitesi
Olağan organik bileşikler üzerindeki reaksiyonlar
SudaSu organomagnesiums reaksiyonu çok (bu bir bir canlı asit-baz reaksiyonu : p K bir ve ekzotermik (RH / R) 50 =). Bu nedenle çalışma modu, cam eşyalar içindeki havanın ve ayrıca yüzeylerin ve çözücülerin tamamen dehidrasyonunu gerektirir. Özel durumlar dışında, bu reaksiyonun parazitik olduğu düşünülür ve organomagnezyumun yok olmasına yol açar.
Organomagnezyumun su üzerindeki reaksiyonu şu şekildedir:
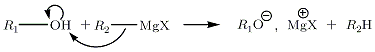 Karboksilik asitlerle
Karboksilik asitlerle
 Aminlerle
Aminlerle
 Terminal alkinler ile
Terminal alkinler ile

Nükleofilik ikame reaksiyonları
Nükleofilik ikame, örnek I 2RMgX'in I 2 üzerindeki nükleofilik sübstitüsyonunu öneriyoruz (bu molekülün polaritesi indüklenir).
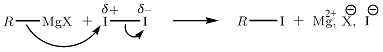 Halojenlenmiş türevlerle nükleofilik ikame
Halojenlenmiş türevlerle nükleofilik ikame
Halojenlenmiş türev: R'-X mekanizması: SN2
R-MgX + R'-X -> RR '+ MgX2
Not: onlar tarafından stabilize olarak UR ve Ar-CH2X ile iyi çalışır endüktif etkisi UR ve mesomer Ar-CH2X için
Epoksilere tepkiMekanizma: SN2
Eterde:
R ---- Mg ---- X + O (CH2) 2 (döngü) → R-CH2-CH2-O-Mg-X
Ardından H3O + asit hidrolizi:
R-CH2-CH2-O-Mg-X + H + → R-CH2-CH2-OH + MgX +
Nükleofilik katılma reaksiyonları ...
... aldehitler ve ketonlarda- Açık aldehit :

İkincil bir alkol oluşumuna organomagnezyum ve aldehitler potansiyel arasındaki reaksiyon, eğer R ' 1 ve R' 2 zincirleri en az bir karbon ihtiva etmektedir. Nihai alkol grubunun destekleyici karbonu asimetrik ise, yani iki R zinciri farklıysa, ürün R ve S konfigürasyonunun iki izomerinden oluşacaktır.
- Açık ketonlar :

Bu reaksiyon, üçüncül bir alkolün oluşmasına yol açar. Aldehitlere gelince, oluşan karbon asimetrik ise, bir R / S 50/50 karışımı elde edilir; bu nedenle stereoseçicilik yoktur. Reaksiyon mekanizmasının incelenmesi, aslında döngüsel bir ara ürün olduğunu göstermektedir:

- Birincil alkol sentezinin özel durumu :
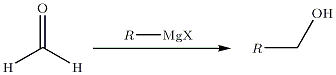 ... esterlerde
... esterlerde
Reaksiyon, bir keton üzerindeki reaksiyona benzer. Hidrolizden sonra, hemiasetali ara yoldan elde ederiz ;
Bu kararsızdır, bir ketona yol açan eliminasyona uğrar. Mevcut organomagnezyum, esterden önce kemoselektif olarak keton ile reaksiyona girecektir, bu daha az reaktiftir, çünkü karbonilinin karbon çekirdeği, tek bir bağ ile bağlanan oksijenin bağlanmayan elektronları tarafından bir şekilde maskelenmiştir. Bu nedenle reaksiyonun genel değerlendirmesi, ara ketonu izole etme olasılığı olmaksızın bir üçüncül alkol oluşumuna yol açar.
... asil klorürler üzerindeReaksiyon, bir keton üzerindeki reaksiyona benzer, ancak daha hızlıdır çünkü klora bağlanan karbon çekirdeği, organomagnezyum radikaline daha çekici bir pozitif yük gösterir.
R ---- Mg ---- X + R'-CO-Cl → R'-CO-R + Cl-Mg-X
Bu nedenle reaksiyon, çok fazla organomagnezyum yoksa izole edilebilir bir keton oluşumuna yol açar. Bu kararsız keton, reaksiyon ortamında bulunan organomagnezyum ajanı ile aşağıdaki reaksiyona göre reaksiyona girecektir: R'-CO-R + RMgX → R-R'COMgX-R ve sonra H2O'nun etkisi altında bir üçüncül alkol elde ederiz. Keton aşamasında durmak istiyorsak, -65 ° C'de çalışmalıyız.
... CO 2'de
Kullanarak karbon dioksit formunda , kuru buz . -40 ° C'deki reaksiyon, bir karboksilik asit R-COOH oluşumuna yol açar.
Notlar ve referanslar
- Victor Grignard , " Bazı yeni organometalik magnezyum kombinasyonları ve bunların alkol ve hidrokarbon sentezlerine uygulanması hakkında ", Académie des science oturumlarının haftalık raporları , cilt. 130, 1900, s. 1322-1325 ( çevrimiçi okuyun )
- (içinde) " The Nobel Prize in Chemistry in 1912 " (erişim tarihi 27 Ekim 2018 ) .




