Protein toplanması
Proteinlerinin toplanması (veya birikme / aglomerasyon proteini ), burada biyolojik bir olgu proteinlerin zayıf katlanmış bir hücre-dışı şekilde içi (biriktikçe ve bir araya toplanır demek olduğunu) agrega. Bu protein kümeleri genellikle hastalıkla ilişkilidir . Gerçekte, protein kümeleri , ALS , Alzheimer ve Parkinson hastalıkları ve prion hastalıkları dahil olmak üzere amiloidoz adı verilen çok çeşitli hastalıklarda rol oynamaktadır .
Sentezlerinden sonra proteinler, kendilerine termodinamik açıdan en uygun olan belirli bir üç boyutlu yapıya katlanma alışkanlığına sahiptir : doğal halleri . Bu katlama işlemi ile tahrik edilir , hidrofobik etki korunmak için deneyin proteinin hidrofobik parça eğilimidir, hidrofilik bir ortamda bir hücre proteini içine kadar delme ile. Bu nedenle, proteinin dışı tipik olarak hidrofilik iken iç kısmı tipik olarak hidrofobiktir.
Protein yapıları, kovalent olmayan bağlar ve iki sistein kalıntısını bağlayan disülfür bağları ile stabilize edilir . Kovalent olmayan etkileşimler arasında iyonik bağlar ve zayıf van der Waals etkileşimleri bulunur . Bir anyon ve bir katyon arasında iyonik etkileşimler oluşur ve proteini stabilize etmeye yardımcı olan tuz köprüleri oluşturur. Van der Waals etkileşimleri polar olmayan etkileşimleri ( Londra kuvvetleri ) ve polar etkileşimleri ( hidrojen bağları , moleküller arası kuvvetler ) içerir. Bu oyun önemli bir rol ikincil yapı gibi bir şekillendirme gibi proteinlerin alfa sarmalı veya beta levha kendi içinde, hem de üçüncül yapı . Belirli bir proteindeki amino asit kalıntıları arasındaki etkileşimler , o proteinin son yapısı için çok önemlidir.
Kovalent olmayan etkileşimlerde, amino asit sekansındaki bir değişiklikten meydana gelebilecek değişiklikler olduğunda, protein muhtemelen kötü bir şekilde katlanacak veya hiç katlanmayacaktır. Bu tür bir durumda, hücre, proteinlerin bu katlanma kusurunu düzeltmesine veya yok etmesine yardımcı olmazsa, bir araya toplanabilirler ve bu süreçte proteinlerin açıkta kalan hidrofobik kısımları, açıkta kalan hidrofobik kısımlarla etkileşime girebilir. proteinler. Oluşabilen üç ana protein agregatı türü vardır: amorf agregatlar, oligomerler ve amiloid fibriller .
Nedenleri
Proteinlerin toplanması çeşitli nedenlerle gerçekleşebilir. Aşağıda ayrıntıları verilen bu nedenlerin kategorize edilebileceği dört sınıf vardır.
Mutasyonlar
Mutasyon meydana gelen sekans arasında DNA ya da proteinin bir amino asit dizisine etki olabilir veya olmayabilir. Sekans etkilenirse, farklı bir amino asit , proteinin katlanmasını etkileyen yan zincirler arasındaki etkileşimleri değiştirebilir . Bu, aynı yanlış katlanmış veya katlanmamış proteinle veya farklı bir proteinle kümelenen proteinin hidrofobik bölgelerinin açığa çıkmasına neden olabilir.
Proteinlerin kendilerini etkileyen mutasyonlara ek olarak, protein agregasyonuna dolaylı olarak katlama yolu ( şaperonlar ) veya ubikitin-proteazom yolu ( ubikitin ligazlar ) gibi düzenleyici yollar sırasında proteinlerde meydana gelen mutasyonlar neden olabilir . Şaperonlar, proteinlerin katlanmaları için güvenli bir ortam sağlayarak katlanmalarına yardımcı olur. Ubikitin ligazları, ubikitinin modifikasyonu ile parçalanacak proteinleri hedefler .
Protein sentezi sırasındaki kusurlar
Protein toplanması, transkripsiyon veya çeviri sırasında ortaya çıkan sorunlardan kaynaklanabilir . Transkripsiyon sırasında, DNA, mRNA'yı oluşturmak için transkripsiyon sonrası değişikliklere uğrayan bir pre-mRNA ipliği oluşturan mRNA'ya kopyalanır . Çeviri sırasında ribozomlar ve RNA'lar , mRNA dizisinin amino asit dizisine dönüştürülmesine yardımcı olur. Hatalı bir mRNA ipliği veya amino asit dizisi üreten bu iki adımdan herhangi birinde kusurlar meydana gelirse, bu, proteinin yanlış katlanmasına neden olarak protein kümelenmesine yol açar.
Çevresel stres
Aşırı sıcaklıklar veya pH veya oksidatif stres gibi çevresel stresler de protein agregasyonuna yol açabilir. Bu tür stresin neden olduğu bir hastalık örneği kriyoglobulinemidir .
Aşırı sıcaklıklar, amino asit kalıntıları arasındaki kovalent olmayan bağları zayıflatabilir ve kararsız hale getirebilir. Belirli bir proteinin pH aralığı dışındaki PH'lar , kovalent olmayan etkileşimleri artırabilen veya azaltabilen amino asitlerin protonasyon durumunu değiştirebilir . Aynı zamanda daha az stabil bağlanmaya ve dolayısıyla proteinin katlanmamasına da yol açabilir.
Oksidatif stres, ROS gibi radikallerden kaynaklanabilir . Bu kararsız radikaller, amino asit kalıntılarına saldırarak yan zincirlerin oksidasyonuna ( aromatik yan zincirler veya metiyonin yan zincirler gibi ) ve / veya polipeptit bağlarının bölünmesine yol açabilir . Bu, proteini doğru şekilde tutan kovalent olmayan bağları etkileyebilir, bu da proteinin dengesizleşmesine neden olabilir ve böylece proteinin katlanmasını önleyebilir.
Yaşlanma
Hücreler, protein kümelerini yeniden katlayabilen veya parçalayabilen mekanizmalara sahiptir. Bununla birlikte, hücreler yaşlandıkça, bu kontrol mekanizmaları daha az etkilidir ve hücre bu kümelerin sorumluluğunu daha az alır.
Protein toplanmasının yaşlanmanın bir sonucu olduğu hipotezi artık test edilebilir çünkü bazı gecikmiş yaşlanma modelleri geliştirilmektedir. Protein agregalarının gelişimi, yaşlanmadan bağımsız bir süreç olsaydı, bu yaşlanmanın yavaşlatılmasının zamanla proteotoksisite oranı üzerinde hiçbir etkisi olmazdı. Bununla birlikte, yaşlanma, proteotoksisiteye karşı koruyucu mekanizmaların aktivitesindeki bir düşüşle ilişkili olsaydı, yavaşlamış yaşlanma modelleri, agregasyon ve proteotoksisitede bir azalma gösterecektir. Bu problemi çözmek için nematod C. elegans'da çeşitli toksisite testleri yapılmıştır . Bu çalışmalar, iyi bilinen bir yaşlanma düzenleyici yol olan insülin / IGF sinyal aktivitesinin azaltılmasının, nörodejenerasyonla ilişkili toksik protein kümelenmesine karşı koruduğunu göstermiştir. Bu yaklaşımın geçerliliği memelilerde test edilmiş ve doğrulanmıştır , çünkü IGF-1 sinyal yolunun aktivitesinin azaltılması, Alzheimer hastalığı olan çalışma farelerini bu hastalıkla bağlantılı davranış ve bozukluklar sergilemekten korumuştur .
Agregaların yeri
Birkaç çalışma, protein agregasyonuna hücresel tepkilerin iyi düzenlendiğini ve organize edildiğini göstermiştir. Protein kümeleri, hücrenin belirli bölgelerinde lokalizedir ve araştırmalar, prokaryotlarda ( E. coli ) ve ökaryotlarda ( maya , memeli hücreleri) bu alanlara odaklanmıştır .
Bakterilerde
Bakteri kümeleri , hücrenin kutuplarından biri olan " eski kutup " da asimetrik olarak bulunur . Hücre bölünmesini takiben , daha fazla ön kutbu içeren yavru hücre, protein kümesini elde eder ve kümesiz yavru hücreden daha yavaş büyür. Bu , bakteri popülasyonu içindeki protein kümelerini azaltmak için bir doğal seçilim mekanizması oluşturur.
Mayalarda
Maya hücrelerindeki çoğu protein agregatının katlanma kusurları şaperonlarla düzeltilir. Bununla birlikte, oksidatif stres tarafından hasar gören proteinler veya bozunmaya yönelik proteinler gibi bazı agregaların katlanma kusurları düzeltilmemiş olabilir. Bunun yerine, iki bölmeden birine yönlendirilebilirler: nükleer membranın yakınındaki JUxtaNuclear Kalite kontrol bölmesi ( JUNQ ) ve maya hücrelerindeki vakuolün yakınında Çözünmez Protein Yatağı veya İngilizce IPOD ) . Protein kümeleri, her yerde bulunduklarında ve bozunmaya yönelik olduklarında JUNQ'a giderken, kümelenmiş ve çözünmeyen proteinler daha uzun depolama için IPOD'a gider. Sonuçlar, bu konumdaki proteinlerin otofaji ile uzaklaştırılabileceğini göstermiştir . Bu iki olasılık, proteazom yolu aşırı yüklendiğinde proteinlerin IPOD'a gitme eğiliminde olacak şekilde birlikte çalışır .
Memeli hücrelerinde
Memeli hücrelerinde, bu protein kümeleri "agresomlar" olarak adlandırılır ve hücre hastalıklı olduğunda oluşur. Bunun nedeni, kümelerin, hücre mutasyona uğradığında meydana gelebilecek heterolog proteinler bulunduğunda oluşma eğiliminde olmasıdır. Ubikitin ligaz E3, yanlış katlanmış proteinleri tanıyabilir ve bunları ubikitin haline getirebilir. HDAC6 sonra ubikuitin ve motor proteini bağlayabilir dinein için agrega "etiketli" taşımak için sentrozom . Oraya vardıklarında, sentrozomu çevreleyen bir kürede kümelenirler. Şaperonlar ve proteazomlar sağlarlar ve otofajiyi aktive ederler.
Agregaların kaldırılması
Hücrede protein kümelerinin uzaklaştırılmasından sorumlu iki ana "kalite kontrol" sistemi vardır. Yanlış katlanmış proteinler, bi-şaperon sistemi tarafından yeniden katlanabilir veya ubikitin-proteazom sistemi veya otofaji tarafından parçalanabilir.
Neo-katlanır
İki şaperon sistemi şaperonlar kullanan Hsp70 (in DnaK-DnaJ-başında grpE , E. coli (ClpB'den ve Hsp100 ve Ssa1-Ydj1 mayada / Sis1-Sse1 / Fe1) , E. coli parçalamak için mayada ve Hsp104) ve neo kat proteinleri.
Hsp70, protein agregaları ile etkileşime girer ve Hsp100'ü görevlendirir. Hsp70, etkinleştirilmiş bir Hsp100'ü stabilize eder. Hsp100, tekli polipeptitleri çözmek için diş açma aktivitesi için kullanılan aromatik gözenek döngülerine sahiptir . Bu diş açma aktivitesi , N-terminalinde , C-terminalinde veya polipeptidin ortasında başlatılabilir . Polipeptit , her biri bir ATP tüketen bir dizi adımda Hsp100 tarafından translokasyona uğrar . Polipeptid katlanmaz ve sonra kendi başına veya ısı şok proteinleri ( ısı şok proteinleri ) yardımıyla yeni katlanmaz .
Bozulma
Yanlış katlanmış proteinler, ubikitin-proteazom sistemi ile uzaklaştırılabilir. Bu, proteinleri bozunmaya yönlendirmek için ubikitinleştiren bir E1-E2-E3 yolundan oluşur. Ökaryotlarda proteinler, 26S proteazomu tarafından bozulur. Memeli hücrelerinde, E3 ligaz ve Hsp70 ile etkileşen karboksi terminal proteini, Hsp70'e bağlı proteinleri hedefler. Mayada, E3 Doa10 ve Hrd1 ligazları, endoplazmik retikulum proteinleri üzerinde benzer işlevlere sahiptir :

Yanlış katlanmış proteinler, protein agregalarının lizozoma taşındığı otofaji ile de çıkarılabilir :
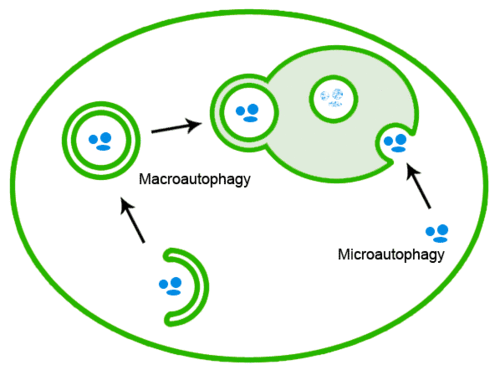
Toksisite
Olgun protein kümelerinin bu şekilde toksik olduğu düşünülse de, son sonuçlar aslında olgunlaşmamış protein kümelerinin en toksik olduğunu ortaya koymaktadır. Bu kümelerdeki hidrofobik gruplar, hücrenin diğer bileşenleriyle etkileşime girebilir ve bunlara zarar verebilir. Hipotezler, protein agregatlarının toksisitesinin, hücresel bileşenlerin sekestrasyon mekanizmaları, ROS üretimi, membrandaki spesifik reseptörlere bağlanma veya membranların bozulması ile ilgili olduğudur. Genetik bir test, daha yüksek moleküler ağırlığa sahip türlerin, zarın geçirgenleşmesinden sorumlu olduğunu belirledi. Protein agregatlarının yapay lipid çift katmanlarını in vitro destabilize edebildiği ve bunun da membran geçirgenleşmesine yol açtığı bilinmektedir .
Ayrıca görün
Notlar
- (fr) Bu makale kısmen veya tamamen alınır İngilizce Vikipedi başlıklı makalesinde " Protein birikimi " ( yazarların listesini görmek ) .
Referanslar
- Adriano Aguzzi ve Tracy O'Connor , " Protein agregasyon hastalıkları: patojenite ve terapötik bakış açıları ", Nature Reviews. Drug Discovery , cilt. 9, n o 3,Mart 2010, s. 237–248 ( ISSN 1474-1784 , PMID 20190788 , DOI 10.1038 / nrd3050 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- Fernanda G. De Felice , Marcelo NN Vieira , M. Nazareth L. Meirelles ve Ludmilla A. Morozova-Roche , " Hidrostatik basınç kullanarak insan lizoziminden ve hastalıkla ilişkili varyantlarından amiloid kümelerinin oluşumu ", FASEB dergisi: resmi yayın Amerikan Deneysel Biyoloji Dernekleri Federasyonu , cilt. 18, n o 10,Temmuz 2004, s. 1099–1101 ( ISSN 1530-6860 , PMID 15155566 , DOI 10.1096 / fj.03-1072fje , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- Rudolph E. Tanzi ve Lars Bertram , " Alzheimer hastalığının yirmi yılı amiloid hipotezi: genetik bir perspektif ", Cell , cilt. 120, n, o , 4,25 Şubat 2005, s. 545–555 ( ISSN 0092-8674 , PMID 15734686 , DOI 10.1016 / j.cell.2005.02.008 , çevrimiçi okuma , erişim tarihi 30 Ekim 2017 )
- MJ Gething ve J. Sambrook , " Hücrede protein katlanması ", Nature , cilt. 355, n o 635502 Ocak 1992, s. 33–45 ( ISSN 0028-0836 , PMID 1731198 , DOI 10.1038 / 355033a0 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- (in) David L. Cox ve Michael Nelson , Lehninger Principles of Biochemistry , New York, WH Freeman,2013( ISBN 978-1-4292-3414-6 ) , s. 143
- Sarah J Shoesmith Berke ve Henry L Paulson , " Protein agregasyonu ve ubikitin proteazom yolu: nörodejenerasyonda UPPer elini kazanmak ", Current Opinion in Genetics & Development , cilt. 13, n o 3,1 st Haziran 2003, s. 253–261 ( DOI 10.1016 / S0959-437X (03) 00053-4 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- (in) Robert F.Weaver, Moleküler Biyoloji , New York, McGraw-Hill,2012( ISBN 978-0-07-352532-7 ) , s. 122-156; 523-600
- Jens Tyedmers , Axel Mogk ve Bernd Bukau , " Protein agregasyonunu kontrol etmek için hücresel stratejiler ", Nature Reviews. Moleküler Hücre Biyolojisi , cilt. 11, n o 11,Kasım 2010, s. 777–788 ( ISSN 1471-0080 , PMID 20944667 , DOI 10.1038 / nrm2993 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- (in) ER Stadtman ve RL Levine , " Serbest amino asitlerin ve proteinlerdeki amino asit kalıntılarının serbest radikal aracılı oksidasyonu " , Amino Asitler , cilt. 25 Kemik yok 3-4,1 st Aralık 2003, s. 207–218 ( ISSN 0939-4451 ve 1438-2199 , DOI 10.1007 / s00726-003-0011-2 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- James F. Morley , Heather R. Brignull , Jill J. Weyers ve Richard I. Morimoto , " Poliglutamin genişleme protein agregasyonu ve hücresel toksisite için eşik dinamiktir ve Caenorhabditis elegans'ta yaşlanmadan etkilenir ", Proceedings of the National Academy of Amerika Birleşik Devletleri Bilimler , cilt. 99, n o 16,6 Ağu 2002, s. 10417–10422 ( ISSN 0027-8424 , PMID 12122205 , DOI 10.1073 / pnas.152161099 , çevrimiçi okuma , erişim tarihi 30 Ekim 2017 )
- Natalia G. Bednarska , Joost Schymkowitz , Frederic Rousseau ve Johan Van Eldere , " Bakterilerde protein toplanması: işlevsellik ve toksisite arasındaki ince sınır ", Mikrobiyoloji (Reading, İngiltere) , cilt. 159, n o Pt 9,Eylül 2013, s. 1795–1806 ( ISSN 1465-2080 , PMID 23894132 , DOI 10.1099 / mic.0.069575-0 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- Mari Takalo , Antero Salminen , Hilkka Soininen ve Mikko Hiltunen , " Nörodejeneratif hastalıklarda protein toplanması ve parçalanma mekanizmaları ", American Journal of Neurodejenerative Disease , cilt. 2, n o 1,2013, s. 1–14 ( ISSN 2165-591X , PMID 23516262 , PMCID PMC3601466 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- (içinde) Rafael Garcia-Mata , Ya-Sheng Gao ve Elizabeth Sztul , " Çöpü Çıkarmadaki Zorluklar: Aggravating Aggresomes " , Trafik , cilt. 3, n o 6,1 st Haziran 2002, s. 388–396 ( ISSN 1600-0854 , DOI 10.1034 / j.1600-0854.2002.30602.x , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- (in) Niels Gregersen Lars Bolund ve Peter Bross , " Protein yanlış katlanma, agregasyon ve hastalıkta bozulma " , Molecular Biotechnology , cilt. 31, n o 21 st Ekim 2005, s. 141–150 ( ISSN 1073-6085 ve 1559-0305 , DOI 10.1385 / MB: 31: 2: 141 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- Axel Mogk , Eva Kummer ve Bernd Bukau , " Protein ayrıştırmada Hsp70 ve Hsp100 şaperon makinelerinin işbirliği ", Frontiers in Molecular Biosciences , cilt. 2,2015, s. 22 ( ISSN 2296-889X , PMID 26042222 , PMCID PMC4436881 , DOI 10.3389 / fmolb.2015.00022 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- Krzysztof Liberek , Agnieszka Lewandowska ve Szymon Zietkiewicz , " Protein ayrışmasının kontrolünde şaperonlar ", The EMBO dergisi , cilt. 27, n o 223 Ocak 2008, s. 328–335 ( ISSN 1460-2075 , PMID 18216875 , PMCID PMC2234349 , DOI 10.1038 / sj.emboj.7601970 , çevrimiçi okuma , erişim tarihi 30 Ekim 2017 )
- Bryan Chen , Marco Retzlaff , Thomas Roos ve Judith Frydman , " Protein kalite kontrolünün hücresel stratejileri ", Cold Spring Harbor Perspectives in Biology , cilt. 3, n o 8,1 st Ağustos 2011, a004374 ( ISSN 1943-0264 , PMID 21746797 , PMCID PMC3140689 , DOI 10.1101 / cshperspect.a004374 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- YJ Zhu , H. Lin ve R. Lal , " Taze ve fibril olmayan amiloid beta proteini (1-40), yaşlı insan fibroblastlarında hızlı hücresel dejenerasyona neden olur: AbetaP kanalı aracılı hücresel toksisite için kanıt ", FASEB dergisi: resmi yayın Amerikan Deneysel Biyoloji Dernekleri Federasyonu , cilt. 14, n o 9,Haziran 2000, s. 1244–1254 ( ISSN 0892-6638 , PMID 10834946 , çevrimiçi okuma , erişim tarihi 30 Ekim 2017 )
- C. Nilsberth , A. Westlind-Danielsson , CB Eckman ve MM Condron , " 'Arctic' APP mutasyonu (E693G), gelişmiş Abeta protofibril oluşumuyla Alzheimer hastalığına neden olur ", Nature Neuroscience , cilt. 4, n o 9,Eylül 2001, s. 887–893 ( ISSN 1097-6256 , PMID 11528419 , DOI 10.1038 / nn0901-887 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- (içinde) Claudio Soto , " Nörodejeneratif hastalıklarda protein yanlış katlanmasının rolünü ortaya çıkarmak " , Nature Reviews Neuroscience , cilt. 4, n o 1,Ocak 2003, s. 49–60 ( ISSN 1471-003X , DOI 10.1038 / nrn1007 , çevrimiçi okuma , 30 Ekim 2017'de erişildi )
- Patrick Flagmeier , Suman De , David C. Wirthensohn ve Steven F. Lee , " Protein Agregalarından Kaynaklanan Lipid Vesiküllere Ca (2+) Akımının Ultrasensitif Ölçümü ", Angewandte Chemie (International Ed. In English) , cilt. 56, n o 27,26 Haziran 2017, s. 7750-7754 ( ISSN 1521-3773 , PMID 28474754 , Bulunamayan PMCID PMC5615231 , DOI 10.1002 / anie.201700966 , çevrimiçi okumak erişilen, Ekim 30, 2017 )
Dış bağlantılar
- (tr) Folding @ Home Help protein katlamanın kodunu çözer.
- (tr) Rosetta @ Home Protein yapılarının ve komplekslerinin tahmin edilmesine yardımcı olur.