Askorbat peroksidaz
L- Askorbat peroksidaz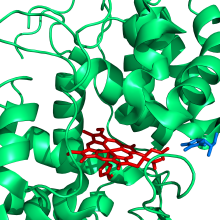 APX Sitosol arasında soya fasulyesi ile kompleks askorbat (mavi), kırmızı gösteren hema bir bağlanmış kalıntı arasında histidin ( PDB 1OAF )
APX Sitosol arasında soya fasulyesi ile kompleks askorbat (mavi), kırmızı gösteren hema bir bağlanmış kalıntı arasında histidin ( PDB 1OAF )
| EC No. | EC |
|---|---|
| CAS numarası | |
| Kofaktör (ler) | Heme |
| IUBMB | IUBMB girişi |
|---|---|
| IntEnz | IntEnz görünümü |
| BRENDA | BRENDA girişi |
| KEGG | KEGG girişi |
| MetaCyc | Metabolik yol |
| PRIAM | Profil |
| PDB | Yapılar |
| GİT | AmiGO / EGO |
Bir L -ascorbate peroksidaz ( APX ) bir bir oksidoredüktaz katalize reaksiyonu :
2 L - askorbat + H 2 O 2+ 2 H + L -ascorbat + L- dehidroascorbat + 2 H 2 O (genel tepki):(a) 2 L- askorbat + H 2 O 2+ 2 H + 2 monodehidroaskorbat + 2 H 2 O ; (b) 2 monodehidroaskorbat L- askorbat + L- dehidroaskorbat (kendiliğinden).Bu enzimler olan sınıf I hem peroksidaz mevcut, bitkiler , algler ve bazı siyanobakteriler . Askorbat peroksidazlar , sitokrom c peroksidazlara güçlü ardışık benzerlik gösterir . Fizyolojik koşullar altında reaksiyon, hemen ürün monodehydroascorbate , indirgenir askorbat ile monodehydroascorbate redüktaz (NADH) ; redüktaz yokluğunda, iki monodehydroascorbate kökleri hızla dismutate askorbat ve içine dehydroascorbate . İle birlikte monodehydroascorbate redüktaz , glutatyon dehidrojenaz, ve glutation redüktaz , askorbat peroksidaz bir bileşenidir glutatiyon-askorbat döngüsü .
Askorbat peroksidazlar, bir elektron vericisi olarak askorbat için yüksek bir özgüllük sergiler, ancak bunların çoğu, aynı zamanda , bazen karşılaştırılabilir kinetiklerle, sınıf III hem peroksidazların daha karakteristik özelliği olan diğer organik substratları oksitleyebilir , bu da bir enzimi şu şekilde sınıflandırmayı zorlaştırabilir. askorbat peroksidaz.
Askorbat peroksidazlar enzimatik mekanizmasına ilişkin bilinenlerin çoğu üzerinde yapılan çalışmalar gelen sitozolik enzim ve bezelye ve soya fasulyesi . Oksidasyon ile gerçekleştirilir bileşik I içeren heme ait aktif bölgesinde daha sonra alt-tabaka iki molekülü ile azaltılır, S , sırayla bunlara bir elektron transfer her biri:
(1) APX + H 2 O 2→ bileşik I + H 2 O ; (2) bileşik I + H S → bileşik II + S • ; (3) bileşik II + H S → APX + S • + H 2 O.Askorbat peroksidaz olması halinde, bileşik I , bir ihtiva eden geçici bir türdür demir atomunu içinde + 4 oksidasyon durumu (ferryl) ve bir pi-katyonik porfirin kökü olduğu gibi, yaban turpu peroksidazı ; bileşik II sadece ferryle içerir.
Notlar ve referanslar
- (inç) Katherine H. Sharp, Martin Mewies Peter CE Moody ve Emma Lloyd Raven , " Askorbat peroksidaz-askorbat kompleksinin kristal yapısı " , Nature Structural Biology , Cilt. 10, n, o , 4, Nisan 2003, s. 303-307 ( PMID 12640445 , DOI 10.1038 / nsb913 , çevrimiçi okuma )
- (in) Emma Lloyd Raven , " Hem peroksidazlarda fonksiyonel çeşitliliği ve substrat spesifikliğini anlamak: askorbat peroksidazdan ne öğrenebiliriz? " , Doğal Ürün Raporları , cilt. 20, n, o , 4, Ağustos 2003, s. 367-381 ( PMID 12964833 , DOI 10.1039 / B210426C , çevrimiçi okuyun )
- (inç) Graham Noctor ve Christine H. Foyer , " ASCORBATE AND GLUTATHIONE: Keeping Active Oksijeni Kontrol Altında Tutmak " , Yıllık İncelemeler , cilt. 49, Haziran 1998, s. 249-279 ( PMID 15012235 , DOI 10.1146 / annurev.arplant.49.1.249 , çevrimiçi okuyun )
- (in) William R. Patterson, Thomas L. Poulos ve David B. Goodin , " Identification of a Porphyrin .pi. Askorbat Peroksidaz Bileşik I içinde Radikal Katyon ” , Biyokimya , cilt. 34, n o 13, Nisan 1995, s. 4342-4345 ( PMID 7703248 , DOI 10.1021 / bi00013a024 , çevrimiçi okuyun )
- (in) Deborah K. Jones, David A. Dalton, Federico I. Rosell ve Emma Lloyd Raven , " Class I Heme Peroxidases: Characterization of Soya Ascorbat Peroxidase " , Archives of Biochemistry and Biophysics , Cilt. 360, n o 2 15 Aralık 1998, s. 173-178 ( PMID 9851828 , DOI 10,1006 / abbi.1998.0941 , çevrimiçi okuma )
