İlerleyici supranüklear felç
Progresif supranükleer felç - PSP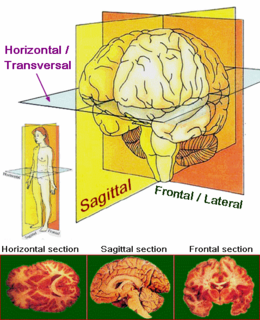 Beynin bölümlerine uygulanan ana anatomik düzlemler ve eksenler.
Beynin bölümlerine uygulanan ana anatomik düzlemler ve eksenler.
| Uzmanlık | Nöroloji |
|---|
| ICD - 10 | G23.1 |
|---|---|
| CIM - 9 | 333.0 |
| OMIM | 601104 |
| Hastalıklar DB | 10723 |
| MedlinePlus | 000767 |
| eTıp | 1151430 |
| eTıp | nöro / 328 |
| MeSH | D013494 |
| İngiltere hastası | Progressive supranuclear-palsy-pro |
Felç progresif supranükleer (PSP veya Steele-Richardson-Olszewski hastalığı , 1963, özelliği doktor isimleri) a, nörodejeneratif hastalık , beynin, çeşitli bölgelerinden nöronların sürekli bir yıkıma striatum , oluşum çapraz bağlı beyin sapı , Nijer lokusu , kraniyal sinirlerin çekirdeği . Bu lezyonlar özellikle PSP'nin özelliği olan vertikal göz sakkadlarının ( supranükleer oftalmopleji ) yapılmasında güçlük yaratırken , yavaş yavaş denge , görme , yürüme , yutma , konuşma ve daha genel olarak sagital düzlemde yapılan hareketleri de etkiler . PSP, etnik köken, yaşam ortamı veya profesyonel faaliyetle bağlantılı herhangi bir risk faktörünü tanımlayamadan, hem erkek hem de kadın olmak üzere 100.000 kişiden yaklaşık altısını etkiliyor . PSP'nin bazı semptomları frontotemporal dejenerasyon , Parkinson hastalığı veya multisistem atrofisine benzer, ancak okülomotor hasar ile ayırt edilir. PSP'nin patolojik mekanizmaları hala tam olarak anlaşılmamıştır: bazen tauopati olarak tanımlanır çünkü nörofibriler dejenerasyon, sinir hücrelerinde bir Tau proteini birikimi ile ilişkilidir .
Keşif
Öncelik arayışı ortasından olasılıkla en az PSP vakalarını uyandırmak rağmen bu durum, 1904 yılında ilk kez tanımlanmıştır XIX inci yüzyıl. Ancak bu olduğunu gözlemler aşağıdaki P r J. Clifford Richardson o davet etmişti ve sonra Toronto 1950 yılında P r John Steele ve P r Jerzy Olszewski (pl) , merkezi sinir sisteminde patolojik değişiklikleri incelemek için PSP olacak o kendi başına bir hastalık olarak tanımlanmakHaziran 1963. Üç nöroloğun çalışmasının 1964 yılında yayınlanmasıyla birlikte, PSP, Amerika Birleşik Devletleri'nde "Richardson-Olszewski hastalığı", "Steele sendromu" adı altında da bilinen özel bir nozolojik varlık olarak şu anki adı altında tanınacak. Avrupa'da ise “Steele-Richardson-Olszewski hastalığı” adı altında.
P r John Steele tarafından da tanımlanan Guam sendromu , Pasifik'teki Guam adasından özel bir PSP formudur . Bu nedenle, genellikle Parkinson hastalığının Amyotrofik Lateral Skleroz ve demans ile ilişkisi olan atipik bir parkinson sendromudur.
Terimin açıklaması
Genellikle "felç", vücudun bir bölümünün motor zayıflığı veya felçidir.
"Supranükleer" terimi, PSP'deki göz probleminin doğasına karşılık gelir. PSP'li bazı hastalar semptomlarını "bulanık" olarak tanımlasa da, asıl sorun, gözbebeklerini hareket ettiren kaslardaki güçsüzlük (veya felç) nedeniyle gözleri doğru şekilde hedefleyememektir. Bu kaslar, beyin sapında beyin tabanının yakınında kümeler veya "çekirdekler" halinde bulunan sinir hücreleri tarafından kontrol edilir.
Göz hareketlerini etkileyen sorunların çoğu beyindeki bu çekirdeklerden kaynaklanır, ancak PSP'de sorun beynin bu çekirdekleri kontrol eden bölümlerinden kaynaklanır. Bu "daha yüksek" kontrol bölgeleri, " supra " ön ekinin "supranükleer" (çekirdeklerin üstünde) anlamına geldiği şeydir .
Patofizyoloji
PSP'den etkilenen beynin ana alanları şunlardır:
- beyin sapı , bir kısmı, özellikle de orta beyinde burada göz kalıntılarının “supranükleer” hareketi, hem de dopaminerjik çekirdekleri;
- bazal gangliyonlar , özellikle subtalamik çekirdek , siyah madde (veya lokus niger ) ve globus pallidus ;
- serebral korteks , frontal lob, özellikle alanı;
- dişli çekirdeği beyincik (serebellum iyi eden nöronların% 50 temsil eder) ;
- ve omurilik , özellikle belirli mesane ve bağırsak kontrollerinin yapıldığı alan.
Epidemiyoloji
PSP nadir görülen bir hastalıktır çünkü 2.000 kişide birden daha azını etkiler ve bu eşiğin altında Avrupa Birliği'nde hastalık nadir olarak tanımlanır. En bildirilen prevalans PSP için yaklaşık 100.000 kişi başına 6 hasta olduğunu. Bu rakam bu güne sadece bir gösterge olarak kalıyor. Halihazırda etkili tedavisi bilinmediği sürece , aynı zamanda bir öksüz hastalıktır . PSP, şiddetli prognozlu bir hastalıktır.
Amerika Birleşik Devletleri ve Avrupa'da on binlerce insanı etkiliyor (tahminlere göre 40.000 ila 60.000). Erkekleri kadınlardan biraz daha fazla etkiler (yaklaşık% 2 fark). Esas olarak 55 ile 65 yaşları arasındaki kişilerde görülür.
Tanı
Semptomlar
En erken semptomlar , epizodik hafıza tutma ile entelektüel yavaşlama , ilgi kaybı ( halsizlik ) veya sinirlilik gibi davranışsal değişikliklerdir . Bu davranış bozuklukları, depresif bir durumu taklit edebilir. Hastalar genellikle düşmelerden sorumlu olan ciddi denge bozukluklarına başvurur. Bu hastalar günde birkaç kez düşebilir; yarı yolda geriye doğru düşer. Hastalar çok dengesizdir ve sandalyeye düşme eğilimindedir. Denge kaybı, yürümeyi zorlaştıracak hatta imkansız hale getirecek kadar kötüleşir.
Sözel akıcılıkta ve konuşma bozuklukları çeşitlidir: (kekemelik palilalia , echolalia ), anlaşılabilir cümleler yayınlanmasında sözlü azim, burun gürültü ve zorluk.
Dikkat bozukluğu: Hasta, uzun süreli bir konuşmayı sürdürmekte güçlük çeker, konuyu birkaç dakika sonra fark etmeden aniden değiştirir. Afaziye doğru eşzamanlı bir evrimle birlikte bu süre konuşmayı imkansız kılacak şekilde kısaltılır .
Denge ve hareketlilik bozukluklarının yanı sıra görsel zorluklar gibi daha sinsi rahatsızlıklar da eklenmektedir. Bu görsel problemler, göz hareketlerini kontrol eden beyin merkezlerinin hasar görmesi nedeniyle gözleri yönlendirememekten kaynaklanmaktadır. Yutma bozuklukları daha sonra ortaya çıkar ve kendileri de pulmoner komplikasyonlara yol açan yiyecek “yanlış yollarına” yol açabilir: Boğulma nedeniyle asfiksi, kursun sonunda sık görülen bir ölüm nedenidir. Hasta için doğru beslenmeyi yanlış yola girmeden sürdürmek için, balgam için trakeal aspiratör kullanımı gibi bir gastrostomi de gerekli hale gelebilir .
Semptomların ortaya çıkma sırası kişiden kişiye değişken olduğundan ve semptomların kendisi diğer patolojilerde ortak olduğundan teşhis güçtür. Klinik olarak postüral bozukluklar, aksiyel parkinson bulguları ve okülomotor bozuklukların önünde tanıdan şüphelenilebilir. Klinik muayenede yukarı bakışta yavaşlık, servikal sertlik, daha genel olarak sagital düzlemde bir motor eksiklik, frontal subkortikal bilişsel bozukluklar ve 3 alkış dizisi gibi tekrarlayan motor hareketleri durdurma zorluğu aranacaktır.
Sagital düzlemdeki motor defisit, dikey oküler zorlukları açıklar, duruş düzeltmesi varsayılan olarak durduğunda spontan geri kalır, yutkunma zorluğu. Okülomotor yetersizlik ayrıca öne doğru düşmelere neden olur, hasta artık yolundaki zeminde engellerin varlığını gizlice kontrol edemez (hastanın ortamının adaptasyonu).
Ana semptomlar ve klinik belirtiler arasında şunları hatırlamalıyız:
- denge bozuklukları düşüşe kadar (erken işaret) ve daha özel olarak geriye doğru gitmektedir,
- Bakışların mıknatıslanması: bakış hareketliliğinin kaybı ve özellikle gözleri yukarıdan aşağıya hareket ettirmede,
- davranış değişiklikleri: yürümede yavaşlama, kelimelerde akıcılık, ilgisizlik, dürtüsellik, saldırganlık, dikkatin dengesizliği ve monoton konuşma,
- kavrama davranışı: eli tutulan nesnelerden gevşetmede zorluk,
- eş zamanlı bir sendromun varlığı: sebat, yargı bozukluğu, problem çözmede zorluklar.
Ek testler
MR beyin bazı karakteristik anormallikleri ortaya çıkarabilir: çıkıntı (sagital) üst kısmının inceltme, serebral peduncles (eksenel kesit), genişleme aralığı 4 inci ventrikül (eksenel kesit) frontal atrofi.
Genel olarak PSP tanısını koyan, lezyonların topografik dağılımına bağlı olarak, yorumu DCB ve bazı Lob tipi FTD'ler gibi diğer taupatilerde ortak olabilecek nöropatolojik incelemedir.
Bugüne kadar, PSP'nin beş çeşidi oluşturulmuştur:
- klasik PSP (en sık) ve diğer dört atipik:
- parkinson tipi PSP (PSP-P);
- yürüyüşün “donmasıyla” saf PSP-akinezi (PSP-PAGF);
- PSP-kortikobazal sendrom (PSP-CBS);
- ilerleyici akıcı olmayan PSP-afazi (PSP-PNFA).
Ayırıcı tanı
Ana ayırıcı tanılar şunlardır:
- Alzheimer hastalığı (AD);
- Parkinson hastalığı (PD);
- dejenerasyon kortikobazal (DCB);
- dejenerasyon frontotemporal (DFT) ya da Pick hastalığı ;
- atrofi birden fazla sistem (AMS).
PSP'nin en azından hastalığın başlangıcında tanınması zor olabilir çünkü ilk bozukluklar, Parkinson ve Alzheimer'ın en iyi bilinenlerinde olduğu gibi diğer nörodejeneratif hastalıklarda da mevcuttur ve aynı zamanda AMS ( Atrophy Multi-Systematized ) gibi. veya PSP'ye çok yakın olan DCB ( Cortico-Bazal Dejenerasyon ). Çok uzun zaman önce, DCB durumunda, deneyimli doktorlar zamanın% 50'sinden fazlasında yanılıyordu.
Tanılama hatası, güçlü eşitsizliklerle birlikte ortalama üç yıldan fazla bir süredir hala önemini korumaktadır. PSP'nin parkinson sendromlarının en az% 5'ini temsil ettiği düşünülmektedir, bu nedenle Parkinson hastalığından sonraki ikinci parkinson sendromu önem kazanmaktadır .
Hastaların elde ettiği oftalmopleji Supranükleer ("görünümün mıknatıslanması" sabitliği ve özellikle dikey alanın azalması), tanı için ilk gözle görülür özelliklerden biri olmaya devam etmektedir. Nitekim gözbebeklerinin felç olmasının sonucu, açıklanamayan ve geriye doğru düşmelere neden olmaktır. Öte yandan, parkinson titremesi yoktur ve semptomlar L-Dopa ile tedaviye dirençlidir .
PSP, evrim süreci bilinen ancak kesin nedeni bilinmeyen parkinson sendromlarından biridir . Parkinson hastalığından, tedaviye çok az yanıt veren veya hiç yanıt vermeyen, daha şiddetli seyri ile ayırt edilir. Kendisine çok benzeyen PSP, DCB gibi kötü prognozlu, kademeli ilerleyen, çok zayıflatıcı ve bugüne kadar sadece semptomları tedavi edilebilen hastalıklardır. Of palyatif bakım beklenemez.
Bazen parkinson artı sendromlar olarak adlandırılan atipik dejeneratif parkinson sendromlarında , özellikle Parkinson hastalığından dopaminerjik tedaviye reaktivitenin düşük olması veya hatta yokluğuyla farklılık gösteren, diğer şeylerin yanı sıra postsinaptik lezyonlardan kaynaklanan, bu nedenle şunları ayırt ederiz:
- sinükleinopatilerde multisistem atrofisi ve Lewy cisimcikli demans ;
- taopatilerde progresif supranükleer felç ve kortikobazal dejenerasyon.
Genetik ve risk faktörleri
PSP kalıtsal değildir . Aslında, bir aile üyesi PSP'ye sahip olduğunda, aynı ailenin diğer üyelerinin PSP semptomları gösterdiği vakaların% 1'inden daha azı vardır. Karşılaştırıldığında, kalıtımsal olmadığı düşünülen bir hastalık için: Parkinson hastalarının% 15'inin etkilenen bir akrabası vardır ve hastaların en az% 5'inin, belirli genlerdeki bir mutasyona bağlı bir Parkinson formuna sahip olduğu kabul edilmektedir.
Kromozom 17'de bulunan H1 haplotip
adı verilen tau protein geninin bir varyantı, PSP'ye bağlanmıştır . Neredeyse tüm PSP'li insanlar bu değişkeni ebeveynlerinin her birinden almıştır, ancak genel nüfusun yaklaşık üçte ikisi de öyle. Bu nedenle, H1 haplotipi, PSP'yi oluşturmak için gerekli gibi görünmektedir, ancak yeterli değildir.
Diğer genler (olası genetik yatkınlıklar ) ve toksik çevresel bileşenlerin yanı sıra hastalığın başlangıcına müdahale ettiğinden şüphelenilen diğer katkıda bulunanlar üzerinde araştırmalar yürütülmektedir .
Guam sendromu ve Guadeloupe dahil Antillerin atipik parkinson sendromları için, bu PSP'ler için, bir gıda faktörü (özellikle tarçın tüketimi) tarafından ek bir risk oluştuğu gösterilmiştir . Ek olarak, Wattrelos'ta arsenik ile önemli kirlilikle ilişkili bir PSP salgını gözlemlendi . İkisinin ortak yanı, güçlü mitokondriyal inhibitörler olmalarıdır. Bu nedenle, tauopatinin yanı sıra, mitokondriyal disfonksiyon bu hastalıkta önemli bir faktör gibi görünmektedir.
Tedavi
PSP belirli profiller için, ve hastalığın başlangıcında, tedaviler, Parkinson hastalığı (üzere uyarlanmış dopamin , rivastigmin , vs. ) kullanılabilir. Bununla birlikte, sonuçlar söz konusu olduğunda, bunlar genellikle zayıf ve her zaman geçicidir. Öte yandan, hasta için alınan herhangi bir kazanımın alındığı unutulmamalıdır.
Mevcut tedaviler, zaman içinde bu nedenle esasen semptomatiktir ve hastalığın neden olduğu rahatsızlık ve seyri ile mücadele etmeye çalışır. Bu nedenle, hastanın ailesi ve çevresi esastır, ancak hastalığın gelişimine göre palyatif bakım ve tedavinin uygulanması için maddi ve manevi düzeyde desteklenmeli ve yardım edilmelidir . Tekerlekli sandalye ve ilgili düzenlemeler, PSP'de oldukça erken bir ekipmandır.
Yetim uyuşturucularla ilgili bir yönetmelik, Avrupa Parlamentosu tarafından şu tarihten beri kabul edilmiştir: 15 Aralık 1999.
Son olarak, FDA ve EMEA'dan ( Amerika Birleşik Devletleri ve Avrupa için iki ilaç kurumu) “yetim uyuşturucu” statüsü aldıktan sonra , iki ilaç, Davunetide ve ZentylorTM serbest bırakılma sürecindedir.PSP'yi kontrol etmek için Faz II denemesi. Yeni biyoteknoloji hükümleri kapsamında hızlandırılmış bir değerlendirme prosedürü için FDA onayı aldılar .
2013'ün başından beri, ne yazık ki, Davunetide için bir faz III denemesinde, ikincil veya keşif sonlanım noktalarının hiçbirinin değişim belirtisi göstermediğini biliyoruz. Her şeye rağmen, bu başarısızlığın bu hastalıkla mücadeleye olumlu katkı payını olacağı umulmaktadır.
Prognoz
Hastalık doğrudan ölümcül olmamakla birlikte, buna sahip olanların yaşam süresini kısaltmaktadır. Bir yandan tanısal hata diğer yandan hastanın yaşı ve genel sağlık durumu göz önüne alındığında, PSP tanısı alan bir hasta için bu yaşam beklentisi nadiren 15 yılı aşmaktadır. Öte yandan, bu alandaki ortalamalar bir hastadan diğerine güçlü eşitsizlikleri yansıtmadığı için önemli değildir. En çok kabul edilen ortalama yaklaşık 7 yıldır. PSP hastalarında yaşam beklentisinin ve hatta ölüm oranının azalmasının ana nedenleri şunlar olabilir:
- kazara geriye doğru düşer, hastalığın özelliği;
- tekrarlayan aspirasyona bağlı solunum yolu enfeksiyonları;
- hastanın genel ve erken tükenmesi, özellikle hasta başka patolojilerden muzdaripse ve yaşlıysa.
Araştırma
Tanı
Post mortem nöropatolojik inceleme / AnatomopatolojiDiğer nörodejeneratif hastalıklarda olduğu gibi, bugüne kadar progresif supranükleer palsinin kesin teşhisine izin veren tek muayene olmaya devam etmektedir. Bu bağlamda, beyinlerini bağışlayan hastalar ve aileleri, PSP ve nörodejeneratif hastalıkların anlaşılması ve bunlarla mücadelede önemli ilerleme sağlanmasına izin verir.
Parkinson hastalarında enterik sinir sisteminde de hasar olduğu tespit edilmiş olsa da, merkezi sinir sistemine verilen hasar ile enterik sinir sistemine verilen hasar arasında bir korelasyon olduğu görülüyor. Bu ilerleme, mevcut ve gelecekteki ilaçların taranması ve geliştirilmesi ve "ayarlanması" açısından dikkate değerdir. Nitekim merkezi sinir sistemine ancak hastaların ölümünden sonra ulaşılabilmektedir. Basit bir biyopsi ile in vivo araştırma yapabilme avantajına sahip olan enterik sinir sistemi gibi periferik sinir sistemlerinde durum böyle değildir . Teşhisin zorluğu böylelikle aşılmış olacaktır.
Diğer yaklaşımlar800 hastayı içeren Avrupa NNIPPS projesi, 2001 yılında PSP'nin klinik, bilişsel, nöro-radyolojik ve histolojik özelliklerini incelemeyi önerdi . 2011'de yayınlanan nihai sonuçlar maalesef denemelerin beklenen etkinlik sonuçlarını vermediğini doğruladı. Durumun özelliği olan okülomotor ve denge bozukluklarının doğası üzerine de araştırmalar yapılmaktadır.
DCB, PSP, Pick hastalığı dahil DFT hastalıkları taupatiler (veya tauopatiler) olarak kabul edilir , tıpkı Alzheimer hastalığı gibi tau proteininin anormalliklerinden kaynaklanan hastalıklar, ilgili hasta sayısı nedeniyle daha iyi bilinir.
Bununla birlikte, nörodejeneratif patolojilerin sınıflandırılması, 1990'ların ortalarından sonlarına kadar daha karmaşık hale geldi.
Moleküler ve genetik yaklaşımlarla, nörodejeneratif hastalıklar için, nöropatolojik lezyonların bileşenlerinin doğasına dayalı olarak yeni bir sınıflandırma ve tanım ortaya çıkmıştır:
- Tauopatıler hastalıkları içerir , protein mikrotübül tau katılmaktadırlar. Tau proteini kümeleri veya çalıları oluşur, birikir ve yayılır, yavaş yavaş kontamine hücrelerin sinirsel ölümüne yol açar. Yetişkinlerdeki ana dejeneratif taupatiler Alzheimer hastalığı, progresif supranükleer felç, kortiko-bazal dejenerasyondur ve bunlar aynı zamanda arjirofilik tahıl hastalığı, Pick hastalığı ve parkinson sendromlu frontotemporal dejenerasyonlarla karşılaştırılır. Kromozom 17 ile bağlantılı.
- Sinükleinopatiler anormal mevduat sahip alfa-sinüklein . Bu presinaptik protein, Parkinson hastalığında lezyonların ve Lewy cisimcikli demansların yanı sıra çoklu sistemik atrofilerin önemli bir bileşenidir. Çoklu sistematik atrofinin glial sitoplazmik kapanımlarında, bir alfa-sinüklein proteinlerinin birikimi de gözlenir.
FKBP52 proteini, yüksek miktarda FKBP52'nin nöronlarda Tau proteinlerinin birikmesini önleyeceği için bir tür anti-Tau proteini görevi görür. Bu nedenle, FKBP52 proteini üzerinde çalışılmaktadır ve ikili bir zorluk vardır: FKBP52 proteini miktarını ölçerek daha iyi taramaya izin vermek ve tau patolojisinin gelişimini bloke etmek için ilaçlar geliştirmek.
Özellikle Tau proteinini hedefleyen stratejilere dayalı olarak, terapötik süreçleri modelleyebilen daha geniş sonuçlar elde etmek için tüm bu deneylere devam edilecektir.
Uygulamalı araştırmada, PSP'ye karşı bir tedavi oluşturabilmek için halihazırda bilinen ancak dozlanan farklı moleküller üzerinde testler yapılmaktadır. Bu lityum (ABD), Q10 (ABD ve İngiltere), için geçerlidir sodyum valproat (Fransa), metiltiyoninyum klorid , vb Bugüne kadar, testin erken aşamalarında en umut verici moleküller için bile, bu ilaçlar beklenen terapötik etkileri sağlamamıştır.
Ayrıca, amiloid ve DNF lezyonları (tau'nun dahil olduğu) tarafından tetiklenen nötr sfingomiyelinaz proteini (N-SMase) üzerindeki testlerden de bahsetmeliyiz, bu protein N-SMase inhibe edildikten sonra apoptotik nöronal ölüm sürecinde etkisiz hale gelecektir. Beklenen sonuç, özellikle Alzheimer hastalığı durumunda hafıza açısından, bu şekilde korunan nöronal sermayeye eşit olacaktır.
Mekanizmalar
Güçlü bir şekilde dahil olan bir protein olan tau proteiniProteinlerin kodlanması, kasıtlı olarak hücrelerimizin normal yaşam ya da ölüm ( apoptoz ) işlevlerini üstlenmek için karmaşık biyokimyasal ve moleküler mekanizmalara uyar .
1980'lerde nörofibriler dejenerasyon , araştırmalar tarafından uzun süredir ihmal edilen tau proteini ile ilişkilendirildi ve şimdi yeni ilgi uyandırıyor.
Tau proteini, diğer tüm proteinler gibi, genlerimiz tarafından kodlanır ve tau proteinini kodlayan gen, kromozom 17 üzerinde bulunur . Her insan, normalde patojenik olmayan ve yaşla birlikte bu hale gelebildiği zaman bile, sinir sisteminde genişlemediği için toksik olmayan tau proteini üretir. Patojenik olmayan durumdan tau proteininden patojene, ardından patojenden toksik duruma geçişi yöneten mekanizmalar açıklanamamıştır.
Hastalığın seyri beyindeki tau ile aynıdır. Tau patolojisinin biyokimyasal ve morfolojik bir nörofibriler dejenerasyon imzası vardır. Öte yandan, etkilenen bir bölge ile belirli bir bilişsel işaret arasında çok kesin bir ilişki beklenemez, çünkü diğer ağırlaştırıcı faktörler söz konusudur.
Ancak, tau patolojisinin, patolojinin klinik belirtiler yönünde gittiği ölçüde bir anlamı olduğu unutulmamalıdır. Örneğin, Alzheimer için: hafıza kaybı ( etkilenen hipokampus ) sonra kademeli olarak afazi ( semantik demansta olduğu gibi etkilenen medyan ve üst temporal korteks , daha sonra dilin farklı alanları olan frontal anterior ve Broca bölgesi ), apraksi ( etkilenen frontal korteks ) agnozi ( paryetal lob , oksipital lob ). Frontal tutulum da davranışsal rahatsızlıklara neden olabilir.
Tau patolojisi kortekste ne kadar ilerlerse, bireysel savunmasızlığa bağlı olarak yol o kadar değişken hale gelir. Birleştirici ve daha sonra birincil korteksin bölgelerinin katılımındaki varyasyon, kişiler arası belirgin klinik varyasyonlara neden olur. Bu nedenle her nörodejeneratif hastalık oldukça kesin ve sabit bir genel ve istatistiksel profile sahiptir, ancak her vakanın kendine özgü bir özelliği vardır. Bu gelişim profili, örneğin Alzheimer hastalığı için, atakların karakteristiği olan 10 aşamada gösterilebilir.
Fransa'da tedavi, bakım ve araştırma organizasyonu
Dan beri Mayıs 2007İlk Nadir Hastalıklar Ulusal Planı çerçevesinde, PSP Fransa birliğiyle bağlantılı olarak , Paris'teki Salpétrière hastanesinde bir referans merkezi progresif supranükleer felç için etiketlendi .
Dan beri Mart 2009, PSP için ulusal referans ve yeterlilik merkezleri ağı, destek, tedavi ve araştırmada ek uzmanlık sağlamayı amaçlamaktadır. Fransa-DFT derneği (DFT için) tarafından 2010 yılının başlarında katılmış olan PSP Fransa derneği (PSP ve DCB için), terimin tıbbi anlamıyla bu ağda nadir demanslar için mevcut olan tek iki hasta derneğidir ve terimin tıbbi anlamı değildir. psikiyatrik (nozolojik sınıflandırma) .
Dan beri 28 Şubat 2011, PNMR (Nadir Hastalıklar Ulusal Planı) yenilendi ve 180 milyon avroluk bir bütçeye sahip.
NeuroSpin merkezini de içeren araştırmalar, nöronal dejenerasyon mekanizmalarını daha iyi anlamayı, onları daha iyi tanımayı ve önlemeyi; bu tür bir hastalığın ilerlemesini daha iyi yavaşlatmak, hatta iyileştirmek için.
Hastalıklı kişilikler
- Peter Sarstedt (1941-2017), İngiliz şarkıcı.
- Abdus Salam (1926-1996), Pakistanlı fizikçi Sheldon Glashow ve Steven Weinberg ile 1979 Nobel Fizik Ödülü'nü aldı .
Notlar ve referanslar
- Charles Dickens (1857), edebiyat ve PSP
- (in) Richardson JC Steele J, Olszewski J, " Supranükleer oftalmopleji, psödobulbar felci, ense distonisi ve demans. Sekiz 'heterojen sistem dejenerasyonu' vakası üzerine bir klinik rapor ” , Amerikan Nöroloji Derneği İşlemleri , cilt. 88, 1963, s. 25–9 ( PMID 14272249 )
- (inç) I. Litvan vd. "Kortikobazal dejenerasyonun klinik tanısının doğruluğu: klinikopatolojik bir çalışma" Neurology 1997: 48: 119-25.
- (in) Samii A Nutt JG, BR Ransom, " Parkinson hastalığı " , Lancet , Cilt. 363, n o 9423,Mayıs 2004, s. 1783–93 ( PMID 15172778 , DOI 10.1016 / S0140-6736 (04) 16305-8 )
- (in) Lesage S Brice A, " Parkinson hastalığı: monojenik formlardan genetik duyarlılık faktörlerine " , Hum. Mol. Süpürge. , cilt. 18, n o R1,Nisan 2009, R48–59 ( PMID 19297401 , DOI 10.1093 / hmg / ddp012 )
- [PDF] Yetim İlaç
- 300 hastayı içeren çok uluslu Davunetide çalışması Amerika Birleşik Devletleri, Avustralya, Almanya, Fransa, Kanada ve Birleşik Krallık'taki büyük tıp kurumlarında yürütülmektedir. [1]
- [PDF] Hızlandırılmış prosedür
- [PDF] Biyoteknoloji dosyası
- Beyin bağışı için açıklayıcı site
- [PDF] PLoS ONE, Eylül 2010 | Cilt 5 | Sayı 9 | e12728
- [PDF] PLoS ONE, Ağustos 2011 | Cilt 6 | Sayı 8 | e22293
- [PDF] cpINSERM 26 Ocak 2010
- [PDF] Tau proteinini hedefleyen strateji , Alzheimer hastalığının yönetimi: güncel veriler ve geliştirilme aşamasında - Mart 2011 Özler
- [PDF] Alzheimer'a karşı yeni hedef
- Annals of the Institut Pasteur / News - Cilt 11, Sayı 2, 6 Nisan 2000, Sayfa 25-45.
- (inç) Delacourte A David JP, Sergeant N et al. "Yaşlanma ve Alzheimer hastalığında nörofibriler dejenerasyonun biyokimyasal yolu" Neurology 1999; 52: 1158-65.
- (inç) A Delacourte A ve L Yoğunlaşması "Mikrotübül düzeneği için faktörler olarak normal ve patolojik Tau proteinleri" Int Rev Cytol. 1997; 171: 167-224.
- [PDF] Ulusal Nadir Hastalıklar Planı 2005-2008
- PSP için Ulusal Referans ve Yetkinlik Merkezleri Ağı
- Ulusal Nadir Hastalıklar Planı 2010-2014
- [PDF] Neurospin 24 Kasım 2006
- "Şarkıcı-söz yazarı Peter Sarstaedt 75 yaşında öldü" , BBC , 8 Ocak 2017
Dış referanslar
- Her Seviyede Beyin : Okunacak Kanadalı Bir Blog.
- Nadir Demanslar için Referans ve Yetkinlik Merkezleri Ağı
- ORPHANET, nadir hastalıklar ve yetim ilaçlar için portal
- PSP 39 - Parkinson Parkinson Sendromları
- PSP Vakfı - Amerika Birleşik Devletleri
- Progresif Supranükleer Felç Derneği - PSP Fransa
Resim Galerisi
-
Orta beyin ve arka beyin (postero-lateral görünüm).
-
Beynin tabanı.
-
Optik kanal , optik kiazma ve optik sinir .
-
Gözün From görsel korteksin .
-
İki retina ve görsel korteks arasındaki optik yolların şeması.