Kalsiyum hidroksit
| Kalsiyum hidroksit | |||
| |||
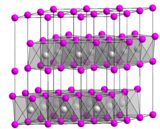
| Kristal yapı. __ Ca2 + __ OH - |
|||
| Kimlik | |||
|---|---|---|---|
| Eş anlamlı |
kalsiyum dihidroksit, kalsiyum |
||
| N O CAS | |||
| K O AKA | 100.013.762 | ||
| N O EC | 215-137-3 | ||
| PubChem | 14777 | ||
| K O D | E526 | ||
| gülümser |
[Ca] (O) O , |
||
| InChI |
InChI: InChI = 1 / Ca.2H2O / h; 2 * 1H2 / q + 2 ;; / p-2 / rCaH2O2 / c2-1-3 / h2-3H |
||
| Görünüm | renksiz kristaller veya beyaz toz | ||
| Kimyasal özellikler | |||
| formül | Ca(OH) 2 | ||
| Molar kütle | 74.093 ± 0.005 g / mol H %2.72, Ca %54.09, O %43.19, |
||
| Fiziki ozellikleri | |||
| T ° füzyon | (ayrışma): 580 ° C | ||
| çözünürlük |
1.85 g · L -1 (su, 0 °C ) 1.73 g · L -1 (su, 20 °C ) |
||
| hacimsel kütle | 2,24 gr · cm -3 | ||
| kristalografi | |||
| kristal sistemi | trigonal kristal sistemi | ||
| Bravais ağı | altıgen Bravais kafes | ||
| ağ parametreleri |
a = 3.589 Å c = 4.911 Å Z = 1 |
||
| Ses | 54.69 A 3 | ||
| Önlemler | |||
| WHMIS | |||
 E, E : Aşındırıcı malzeme. Kuvvetli baz (doymuş bir çözeltinin pH'ı = 12.5). İçerik açıklama listesine göre %1.0 oranında açıklama. |
|||
| Ulaşım | |||
Tanınmayan etiket. Hata bildir: Chat_Model: ADR Etiketi tanınmadı. Hata bildir: Chat_Model: ADR Etiketi tanınmadı. Hata bildir: Tartışma_Model: ADR |
|||
| Aksi belirtilmedikçe SI ve STP birimleri . | |||
Kalsiyum hidroksit a, kimyasal madde , mineral , iyonik bileşiğin katyon kalsiyum ve anyon hidroksit (OH), Ca, ampirik formülü 2. Bu alkali antik da "denir sönmüş kireç ", "yağlı kireç" ve bu aşındırıcı ve bir higroskopik toz hazırlandı için "kireç" sönmemiş kireç ya da kalsiyum oksit , eski üretilen kireç fırını içinde kireç brülör . Aynı zamanda "denilen nadir bir doğal maden, yoğunluk 2.23 olduğunu portlandit tarafından" mineraloglar bunun basit bir üründür, çünkü hidroliz ait Portland çimentosu .
Çözünmüş kireç suyundaki veya kireç sütündeki süspansiyondaki ana bileşendir . Aslında, bu inorganik hidroksit alkali toprak suda yüksek oranda çözünmez: endüstriyel sönmüş kireçlerin bileşimine göre, genellikle biraz magnezya, 1.1 g · L -1 ve 1.6 g · L -1 ila 20 °C arasında, yaklaşık 0.6 g · L -1 ve 0,7 g · L -1 ila 80 °C . Laboratuardaki saf bileşik, ancak biraz daha fazla çözünür. Suda zaten çok düşük olan çözünürlüğü sıcaklıkla biraz azalır. Çözünürlük ürün sabiti 5.02 × 10 -6 ila 25 ° C mertebesindedir .
Hazırlık
Sönmüş kireç, sönmemiş kireç - CaO söndürülerek eski kireç satıcılarının hızlı yöntemine göre hazırlanmıştır.- suya daldırarak. Bu çok ekzotermik bir reaksiyondur, kalsiyum oksidin hidrasyonu kalsiyum hidroksit üretir:
Beyaz katı CaO + H 2 Osıvı → zayıf çözünmüş Ca (OH) 2 (sulu), çoğu su içinde süspansiyon halinde , ΔH = ~ 1 155 kJ · kg -1 sönmemiş kireç ile.Su içinde süspansiyon halinde bölünen 100 g · L- 1 katı "kireç sütü" denilen şeyi oluşturur, kalsiyum hidroksit bir fırında veya fırında kurutulduktan sonra elde edilen beyaz katıdır. Filtrelenmiş kireç sütü berrak bir "kireç suyu" verir. Nemli havada, bir reaksiyon havaya kireci , aslında kalsiyum hidroksit verebilir , ancak bu sadece karbonatlaşma veya karbon dioksitin fiksasyonu olmadığında , ki bu nadiren olur. Kireç suyu bu son gazın varlığında bulanıklaşır: Jean-Baptiste Van Helmont'un çalışmasını takiben eski kimyagerler içindi , bu orman gazının varlığıyla bilinen ilk gaz dedektörü .
Kesinlikle kârsız, ancak laboratuvarda oldukça yaygın olan bir başka radikal yol, metal kalsiyumun reaksiyona girerek bir gaz salınımı meydana getirmesidir:
Ca katı metal + 2 H 2 Osıvı → sulu Ca (OH) 2 , daha sonra büyük oranda taneler halinde çöktürülür + H 2 gazıMetalin potansiyel reaktivitesi ve hidrojen gazının havada patlayıcılığı veya potansiyel yanıcılığı nedeniyle tehlikelidir .
Toksikoloji ve Güvenlik
Aşındırıcı ve cildi ve mukoza zarlarını tahriş ettiği kabul edilen agresif bir alkalidir. Projeksiyon ve/veya temas halinde tahrişe ve özellikle ciddi göz hasarına neden olabilir. Solunum yollarını tahriş eder. Belirli kimyasal düzenlemelerden yoksun, vücudun belirli organlarına yönelik bir toksikoloji sunar. Kronik toksisite hala bilinmemektedir: dişlerin yavaş yavaş zayıflaması gibi uzun vadeli etkilere karşı hassastır.
Çevre için, genellikle sönmüş kireç, özellikle su yolları ve su kütleleri ve sulu ekosistemler için alkali bir tehdittir.
kullanır
Eğer sönmemiş kireç CaO çelik endüstrisinde, bayındırlık işlerinde ve yollarda (Roma Antik Çağ'dan beri yolun tabanının boşaltılması), su arıtma ve tarım, inşaat ve inşaat işlerinin çoğunu üstlenir, sönmüş kireç bir karbondioksit emilim maddesi olarak kullanılır, İster acil anestezide, ister solunum cihazında, ister gıdada.
Kalsiyum hidroksit, birçok üründe gıda pH düzenleyicisi ve sıkılaştırıcı / stabilizatör olarak kullanılan bir gıda katkı maddesidir ( E526 ) .
Kireç, endüstriyel gres üretiminde de kullanılır.
Referanslar
- KALSİYUM HİDROKSİT , Kimyasal Maddelerin Güvenliğine İlişkin Uluslararası Programın güvenlik sayfa(lar)ı, 9 Mayıs 2009'da danışıldı
- hesaplanan moleküler kütlesi " Elements 2007 Atom ağırlıkları " üzerine www.chem.qmul.ac.uk .
- “Kalsiyum hidroksit” in Tehlikeli Maddelerin Veri Bankası (Eylül 21, 2009 erişilir).
- " Kalsiyum hidroksit kimyasal ürünlerin veritabanındaki" Reptox ait CSST 25 Nisan 2009 erişilen (iş güvenliği ve sağlığı sorumlu Quebec örgütü),
- saf laboratuar ürün için, su içinde çözünürlük civarındadır 1.85 g · L -1 de 0 ° C ; 1.28 g · L -1 ila 50 °C ; 0.71 g · L -1 ila 100 °C .
- kutusu
- Kireç yine de ve her şeyden önce, inşaat ve yapısal işlerde çalışan duvarcılar veya profesyoneller için, hidrolik kireç veya hidrolik sertleşen, yani su ile ve muhtemelen daha sonra havada az çok hızlı sertleşen bir hidrolik kireç veya bağlayıcı olarak kalır. İdeal harç, neredeyse anında bir su akışında donan bir kireç olacaktır.
- Hava, hava kireci veya duvar ustaları ve diğer profesyoneller tarafından elde edilen ikinci kireçten farklı olarak, her şeyden önce, özellikle karbonasyon veya karbon fiksasyonu ile havada az veya çok yavaş sertleşen, zayıf nemlendirilmiş kireç veya kireç sütü bazlı bir bağlayıcıdır. dioksit.
- Avrupa Parlamentosu ve Avrupa Konseyi , " Renkler ve tatlandırıcılar dışındaki gıda katkı maddelerine ilişkin 95/2/EC sayılı Direktif ' Avrupa Birliği Resmi Gazetesi , n o L 61,20 Şubat 1995, s. 1-56 ( çevrimiçi okuyun [PDF] ).
- " Gıda katkı maddeleri için sınıf adları ve uluslararası numaralandırma sistemi " [PDF] , CAC/GL 361989 , http://www.codexalimentarius.net , Codex alimentarius ,1989( 14 Eylül 2008'de erişildi ) , s. 1-35
- (in) Gıda Kodeksi Komisyonu , " Kalsiyum hidroksit için Oturum Gıda Kodeksi Komisyonu 31 (526) kadar Güncelleme " , GSFA Çevrimiçi üzerinde http://www.codexalimentarius.net , Codex Alimentarius,2008( 3 Ekim 2008'de erişildi )
Şuna da bakın:
İlgili makale
Dış bağlantılar
- Kireç sayfası
- Toksikolojik levha , CNESST
- Kompakt Kimyasal Güvenlik Bilgi Formu , CDC ,10 Eylül 2015
- Lucile Goupy , " Uzun Süreli Kalsiyum Hidroksit Kullanımıyla İlişkili Riskler " [PDF] , cpeastudyclub.org üzerinde , L'Information dentaire n o 16,16 Nisan 2008