Oksaziridin
| Oksaziridin | |
| Kimlik | |
|---|---|
| IUPAC adı | Oksaziridin |
| N O CAS | |
| PubChem | 15817734 |
| GÜLÜMSEME |
C1NO1 , |
| InChI |
InChI: InChI = 1S / CH3NO / c1-2-3-1 / h2H, 1H2 InChIKey: SJGALSBBFTYSBA-UHFFFAOYSA-N |
| Kimyasal özellikler | |
| Kaba formül |
C H 3 N O [İzomerler] |
| Molar kütle | 45.0406 ± 0.0015 g / mol C% 26.67, H% 6.71, N% 31.1, O% 35.52, |
| Aksi belirtilmedikçe SI ve STP birimleri . | |
Oksaziridinler sınıfıdır organik bileşikler Heterocyclic bir atomu ihtiva eden üç karbon karbon , bir atomu nitrojen ve bir atom oksijen . Oksaziridin CH 2 NHOaynı zamanda fonksiyonel grubun ana bileşiğidir .
Genel Özellikler
İlk oksaziridin türevleri 1950'lerde Emmons, Krimm ve Horner ve Jürgens tarafından sentezlendi . Oksijen ve nitrojen atomları , yüksek elektronegatiflikleri nedeniyle genellikle nükleofil görevi görürken , oksaziridinler iki heteroatomun elektrofilik transferine izin verir . Bu özel reaktivite, oldukça kısıtlanmış üç atomlu halkanın varlığından ve NO bağının göreceli zayıflığından kaynaklanmaktadır. Nükleofiller nitrojen atomu üzerinde ikame küçük olduğunda oksaziridinin nitrojen üzerinde saldırma eğiliminde (tipik olarak R 1 = H) ve atomu nitrojen üzerinde ikame çok oksijen sterik olarak engellenmiş . Bu elektronik etkiler, bir α-hidroksilasyonu gibi çeşitli oksijen ya da azot atomu transfer reaksiyonları yürütmek için kullanılabilir enolatlar , epoksidasyonu ve alkenler veya seçici oksidasyonu sülfürler ve selenürler. .
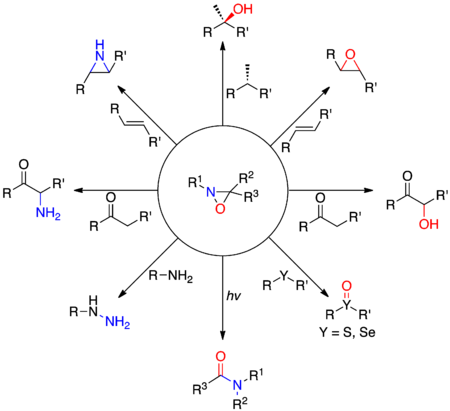
Kiralite
Oksaziridinlerden türetilen kiral reaktifler geliştirilmiştir ve stereospesifik heteroatomların transfer reaksiyonlarına izin verir . Oksaziridinlerin kiralitesi, halkanın ikame edicilerinin yapısından veya nitrojen atomunun ( invertomer ) konformasyonundan gelebilir . Aslında oksazirinler, stereokimyasal konfigürasyonlarının korunmasına izin veren çok yüksek nitrojen inversiyon bariyeri nedeniyle benzersizdir . Oda sıcaklığına bu bariyer dönüşümü 24 ila 31 kcal · mol- 1 düzeyindedir ve enantiyopür oksaziridinler 1980'lerde hazırlanmıştır .
Göre oksaziridinlerin türevleri kafur türevleri sentezlenmiştir 1970'lerin ve bir taşı haline gelmiştir asimetrik sentez . Oksaziridinleri kullanan birçok toplam sentez arasında, taksolün Holton ve Wender ekipleri tarafından toplam sentezi, bu antikanser maddesinin sentezinde anahtar adım olarak kamforsülfoniloksaksiridin ile asimetrik a-hidroksilasyon önermektedir.
Sentez
NH, N-Alkil, N-Ariloksaziridinler
NH, N-alkil ve N-Aryloxaziridines (A) sentezi için iki temel strateji oksidasyon arasında iminler ile perasitler ve (B) aminasyon arasında karbonillerin .

Ek olarak, kiral iminlerin oksidasyonu ve iminlerin kiral perasitler ile oksidasyonu, enantiyomerik olarak saf oksaziridinlerin hazırlanmasına yol açabilir .
N-Sülfoniloksaziridinler
1980'lerin başında ilk N-sülfoniloksaziridin hazırlandı. Bu sülfonil türevleri , yalnızca oksijen atomu transfer reaksiyonları için kullanılır ve şu anda en yaygın kullanılan oksaziridin sınıfıdır. Başlangıçta bir faz transfer katalizörü olarak m-CPBA ve benziltrimetilamonyum klorürden hazırlanmış olup, sentezdeki bir gelişme artık bir oksidan olarak potasyum hidrojenopersülfat veya Okson kullanımına izin vermektedir .
Her biri farklı fizikokimyasal özelliklere ve reaktivitelere sahip olan çok sayıda N-sülfoniloksaziridin türevi kullanılmaktadır. Bu farklı reaktiflerin bir özeti aşağıdaki tabloda sunulmaktadır.

Perflorlu oksaziridinler
Perflorlanmış (in) oksaziridinler , eşdeğer hidrokarbonlarına kıyasla güçlü reaktivite sergiler . Perfluorinatlı ikame benzer perflorlanmış oksaziridinlerin reaktivitesini hale elektron akseptörleri vardır dioksiranların . Perfloroalkiloksaziridinler özellikle belirli CH bağlarını çok yüksek seçicilikle hidroksile edebilir . Perfluorinatlı oksaziridinler bir reaksiyona sokulması suretiyle sentezlenebilir perflorlanmış imin perfluoromethylfluorocarbonyl peroksit ve temizlemek için florlanmış metal ile HF yayınlandı.

Tepkiler
Oksijen atom transferleri
enolatların α-HidroksilasyonuA- hidroksketon grubu veya asilino , birçok doğal üründe bulunan bir birimdir. Bir çok sentetik rotalar gibi, bu motifi yeniden oluşturmak için kullanılmış olan indirgeme α-deiketones bölgesinin ikame hidroksillerin bir için ayrılan grup ya da bir doğrudan oksidasyonu enolat . İkinci yöntemde, oksodiperoksimolibdenum (piridin) - (heksametilfosforik triamid) (MoOPH) ve N-sülfoniloksaziridinler en yaygın kullanılan elektrofilik oksijen kaynaklarıdır . N-sülfoniloksaziridinler, MoOPH ve diğer oksidanların kullanımına kıyasla daha fazla kiralite indükleme avantajına sahiptir. Şiral indüksiyon, SAMP ve RAMP gibi şiral yardımcı maddeler içeren diğer birçok şiral keton ve keton ile gösterilmiştir .

Çalışma asimetrik hidroksilasyon üzerinde yapılmıştır prokiraf enolatlar mümkün iyi ulaşmak için yapım kamforsülfoniloksaziridin türevleri ile enantiyomerik aşırılıkları . Yaygın olarak kabul edilmektedir geçiş durumu mümkün bu iyi bir stereo elde edilmesini mümkün kılar sterik grup molekülü yaklaştı edildiği yan belirler engellenmiş bir açık geçiş durumunu kapsar.

Seçiciliği bazılarının hidroksillenmeler eklenerek geliştirilebilir koordine grupları oksaziridinlerin olarak, oksaziridin halkasının alfa pozisyonunda 3b ve 3c , yukarıdaki tabloda. Reaksiyon, bir gider önerilmektedir kapalı geçiş durumunun metali oksianyon stabilize edildiği şelasyon sülfat sayesinde ve koordinasyon gruplarıyla kafur .

Oksaziridinlerle a-hidroksilasyon, toplam sentezde çok yaygın olarak kullanılmıştır . Bu önemli bir adım olan Holton ile taksan toplam sentezi (in) ve Wender ile taksan toplam sentezi (en) . Benzer şekilde, Forsyth bu reaksiyonu okadaik asidin C3-C14 sisteminin (1,7-dioksaspiro [5.5] undec-3-ene ikameli) sentezinde kullanır .
 Alkenlerin epoksidasyonu
Alkenlerin epoksidasyonu
Epoksidasyon ve alkenler yaygın olarak kullanılan organik sentez epoksitler çok dönüşmüş edilebildiğinden, fonksiyonel grup . Genellikle, epoksidasyon m-CPBA (veya diğer perasitler ) kullanır, ancak oksaziridlerin benzer sentezleri gerçekleştirmek için kullanılabildiği ve asidik koşullara duyarlı epoksitlerin hazırlanmasında çok yararlı olduğu gösterilmiştir . Aşağıda, sentezinin son aşamalarından birinde bir alkenin oksaziridin tarafından epoksidasyonunu kullanan (-) - chaetominin sentezi açıklanmaktadır.

Organik sentez işleme sınıfında yaygın olarak kullanılan bir başka , Sharpless epoksidasyonu , Jacobsen epoksidasyonu veya Julia-Colonna'nın (en) epoksidasyonu gibi asimetrik epoksidasyondur . Bu reaksiyonların en büyük dezavantajı, seçici olmaları için çok özel işlevlere ihtiyaç duymalarıdır . Keskin olmayan epoksidasyon alilik alkollerle , Jacobsen'in aromatiklerle sis- disübstitüe alkenlerle epoksidasyonu ve doymamış α-β ketonların Juliá-Colonna epoksidasyonuyla çalışır . Asimetrik oksaziridinlerin kullanılması mümkün yürütmek için yapar stereo- dönüşümler üzerinde işlevsiz bir alkenler . Aşağıda yer alan Şema trans- asimetrik epoksidasyon stilben kullanarak kiral bir oksaziridinyum tuzu ile okson bir oksidan olarak.
 Devre Dışı Bırakılmış Hidrokarbon Hidroksilasyon
Devre Dışı Bırakılmış Hidrokarbon Hidroksilasyon
Oksaziridinler perflorlanmış (tr) bilinmektedir hidrokside hidrokarbonlar yüksek olan devre dışı regiosterero ve diastéréospécificité . Bu reaksiyon çok önemlidir ve çok az başka bileşik bu tip bir reaktivite sergiler. Perflorlu oksaziridinler, üçüncül karbonlara karşı çok iyi seçicilik sergiler . Birincil karbonların hidroksilasyonu veya iki oksitlenebilir bölgeye sahip bileşiklerin dihidroksilasyonu hiçbir zaman gözlenmemiştir. Stereokimyanın tutulması çok yüksektir,% 95 ila% 95 arasındadır ve bir florür tuzu ilave edilerek daha da arttırılabilir .

Azot atom transferleri
Nitrojen atom transfer reaktifleri olarak oksaziridinlere daha az önem verilmiştir. Sübstitüe edilmemiş veya nitrojen üzerinde bir asil grubuna sahip olan oksaziridinler , ilk örnek 1960'lardan kalma bu tür reaksiyonlar için kullanılabilir .
N-nükleofillerin AminasyonuAminasyon ve nükleofillerle nitrojen üzerinde ikame edilmemiş oksaziridinlerin ile oldukça çok yönlü kullanılabilir nükleofiller görmektedir. Hidrazinler , böylece bir hazırlanabilir aminler , ikincil veya üçüncül aminler, hidroksilaminler itibaren ve thiohydroxylamines alkoller ve tiyoller , sülfilimin gelen tioeterler ve α-aminoketonları itibaren enolatlar .
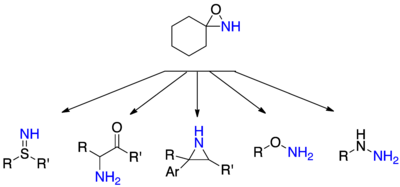 N-asilamidasyon
N-asilamidasyon
Asillenmiş aminlerin transferi ikamesiz aminlere göre daha zordur. Bu transfer reaksiyonları ilk olarak aminler ve hidrazinler gibi nükleofiller kullanılarak gerçekleştirildi . Asillenmiş aminlerin nükleofilik karbonlara transferlerinin birkaç nadir örneği de tarif edilmiştir.

Yeniden düzenlemeler
Oksaziridinler, ultraviyole ışınlama altında , bir radikal mekanizma yoluyla veya CuI gibi bir indirgeme ajanı varlığında yeniden düzenleme reaksiyonlarına girebilir .. Spirosiklik oksaziridinler ayrıca karşılık gelen laktamı vermek için döngülerini uzatabilirler . İkame migrasyonu stereoelektronik etkiler ile kontrol edilir, ve trans- grubu arasında olmayan nitrojen çift bağlama esas olarak geçiş ürün elde edilir. Bu etki, aşağıdaki diyagramda gösterildiği gibi yeniden düzenlemeyi yönlendirmek için yüksek nitrojen ters çevirme bariyeri nedeniyle nitrojenin kiralitesinin kullanılmasını mümkün kılar. Diyagramın sol tarafında sadece termodinamik açıdan elverişsiz ürün gözlemlenirken, diyagramın sağ tarafında daha az kararlı radikal ara maddeden türetilen ürün tercih edilir.

Yeniden düzenlemenin Bu tür kilit aşamada kullanılır toplam sentez (+) - ve yohimbin , karşı etkili olabilen doğal ilaç iktidarsızlık ve cinsel kaynaklanan sorunlar selektif serotonin geri alım inhibitörleri göre ilaç. Ulusal Sağlık Enstitüleri .

Termal yeniden düzenleme tepkimeleri verirler oksaziridinler elde nitronlar . Cis-trans seçiciliği düşüktür, ancak verimler iyidir. Aynı zamanda, belirli oksaziridinlerin bir nitron ara ürününden geçerek zamanla rasemize olduğu da düşünülmektedir .

Heterokümülenli sikloidler
Oksaziridinler, aşağıdaki şekilde gösterildiği gibi farklı beş atomlu heterosikller vermek için hetero kümülenler ile reaksiyona girebilirler . Bu reaktivite, üç atomlu halkanın kısıtlaması ve NO bağının zayıflığından kaynaklanmaktadır.

Notlar ve referanslar
- hesaplanan moleküler kütlesi " Elements 2007 Atom ağırlıkları " üzerine www.chem.qmul.ac.uk .
- (in) WD Emmons , " The synthesis of oxaziranes " , J. Am. Chem. Soc. , cilt. 78, n o 23,1956, s. 6208–6209 ( ISSN 0002-7863 ve 1520-5126 , DOI 10.1021 / ja01604a072 ).
- (de) H. Krimm , " Uber Isonitrone " , Chem. Ber. , cilt. 91, n o 5,1958, s. 1057-1068 ( ISSN 0009-2940 , DOI 10.1002 / cber.19580910532 ).
- (de) L. Horner ve E. Jürgens , " Notiz Über Darstellung und Eigenschaften Einiger Isonitrone (Oxazirane) " , Chem. Ber. , cilt. 90, n o 10,1957, s. 2184–2189 ( ISSN 0009-2940 , DOI 10.1002 / cber.19570901010 ).
- (en) FA Davis ve AC Sheppard , " Oksaziridinlerin organik sentezdeki uygulamaları " , Tetrahedron , cilt. 45, n o 18,1989, s. 5703–5742 ( DOI 10.1016 / S0040-4020 (01) 89102-X ).
- (in) FA Davis , R. Jenkins vd. , " 2 - [(-) - Kafur-10-ilsülfonil] -3- (nitrofenil) oksaziridin: yeni bir kiral oksitleme maddesi " , J. Chem. Soc., Chem. Yaygın. ,1979, s. 600-601 ( ISSN 0022-4936 , DOI 10.1039 / C39790000600 ).
- (inç) RA Holton , C. Somoza ve diğerleri. , “ Taksolün ilk toplam sentezi. 1. B halkasının işlevselleştirilmesi ” , J. Am. Chem. Soc. , cilt. 116, n, o , 4,1994, s. 1597–1598 ( ISSN 0002-7863 ve 1520-5126 , DOI 10.1021 / ja00083a066 ).
- (inç) RA Holton , HB Kim vd. , “ Taksolün ilk toplam sentezi. 2. C ve D halkalarının tamamlanması ” , J. Am. Chem. Soc. , cilt. 116, n, o , 4,1994, s. 1599-1600 ( ISSN 0002-7863 ve 1520-5126 , DOI 10,1021 / ja00083a067 ).
- (inç) PA Wender , NC Badham ve diğerleri. , " Taksanlara giden pinen yolu. 5. Çok yönlü bir taksan öncüsünün stereo kontrollü sentezi ” , J. Am. Chem. Soc. , cilt. 119, n o 11,1997, s. 2755–2756 ( ISSN 0002-7863 ve 1520-5126 , DOI 10.1021 / ja9635387 ).
- (in) PA Wender , NC Badham ve diğerleri. , " Taksanlara giden pinen yolu. 6. Kısa bir stereo kontrollü taksol sentezi " , J. Am. Chem. Soc. , cilt. 119, n o 11,1997, s. 2757–2758 ( ISSN 0002-7863 ve 1520-5126 , DOI 10.1021 / ja963539z ).
- (in) FA Davis ve OD Stringer , " Oksaziridinlerin Kimyası. 2. Geliştirilmiş 2-sülfoniloksaziridin sentezi ” , J. Org. Chem. , cilt. 47, n o 9,1982, s. 1774–1775 ( ISSN 0022-3263 ve 1520-6904 , DOI 10.1021 / jo00348a039 ).
- .
- (en) FA Davis ve BC Chen , " Enolatların N-sülfoniloksaziridinlerle asimetrik hidroksilasyonu " , Chem. Rev. , cilt. 92, n o 5,1992, s. 919–934 ( ISSN 0009-2665 ve 1520-6890 , DOI 10.1021 / cr00013a008 ).
- (in) FA Davis ve RH Jenkins , " Oksaziridinlerin Kimyası. 3. Organosülfür bileşiklerinin kiral 2-sülfoniloksaziridinler kullanılarak asimetrik oksidasyonu ” , J. Am. Chem. Soc. , cilt. 104, n o 20,1982, s. 5412–5418 ( ISSN 0002-7863 ve 1520-5126 , DOI 10.1021 / ja00384a028 ).
- (en) FA Davis , RT Reddy vd. , " Oksaziridinlerin kimyası. 15. 3-ikameli 1,2-benzizotiyazol 1,1-dioksit oksitler kullanılarak asimetrik oksidasyonlar ” , J. Org. Chem. , cilt. 56, n o 21991, s. 809–815 ( ISSN 0022-3263 ve 1520-6904 , DOI 10.1021 / jo00002a056 ).
- (inç) JC Towson , MC Weismiller ve diğerleri. , " (+) - (2R, 8aS) -10- (Camphorylsulfonyl) oxaziridine " , Org. Synth. , cilt. 69,1990, s. 158 ( ISSN 0078-6209 ).
- (in) FA Davis ve JC Towson , " Oksaziridinlerin Kimyası. 11. (Camphorylsulfonyl) oxaziridine: sentez ve özellikler ” , J. Am. Chem. Soc. , cilt. 110, n o 25,1988, s. 8477–8482 ( ISSN 0002-7863 ve 1520-5126 , DOI 10.1021 / ja00233a025 ).
- (en) RD Bach , BA Coddens ve diğerleri. , " Bir oksaziridinden bir sülfite ve bir sülfoksite oksijen transferinin mekanizması: teorik bir çalışma " , J. Org. Chem. , cilt. 55, n o 10,1990, s. 3325–3330 ( ISSN 0022-3263 ve 1520-6904 , DOI 10.1021 / jo00297a062 ).
- (in) FA Davis , A. Kumar ve ark. , " Oksaziridinlerin kimyası. 16. (+) - [(8,8-dimetoksikamphoril) sülfonil] oksaziridin kullanılarak γ-rodomikiyonon ve a-sitromisinin AB-halka segmentlerinin kısa, yüksek oranda enantioselektif bir sentezi ” , J. Org. Chem. , cilt. 53, n o 3,1991, s. 1143–1145 ( ISSN 0022-3263 ve 1520-6904 , DOI 10.1021 / jo00003a042 ).
- (en) FA Davis , MC Weismiller ve diğerleri. , " Yeni optik olarak saf (kamforilsülfonil) oksaziridin türevlerinin sentezinde (Kafurilsülfonil) imin dianyonu " , Tetrahedron Lett. , cilt. 30, n o 13,1989, s. 1613-1616 ( ISSN 0040-4039 , DOI 10.1016 / S0040-4039 (00) 99534-0 ).
- (içinde) BC Chen , MC Weismiller ve diğerleri. , " (+) - kjellmanianonun enantiyoselektif sentezi " , Tetrahedron , cilt. 47, n o 21991, s. 173–182 ( ISSN 0040-4020 , DOI 10.1016 / S0040-4020 (01) 80914-5 ).
- (en) VA Petrov ve G. Resnati , " Poliflorlu oksaziridinler: Sentez ve reaktivite " , Chem. Rev. , cilt. 96, n o 5,1996, s. 1809–1824 ( ISSN 0009-2665 ve 1520-6890 , DOI 10.1021 / cr941146h ).
- (inç) DA Evans , Bay Morrissey ve ark. , " Kiral imid enolatların asimetrik oksijenasyonu. Enantiyomerik olarak saf a-hidroksi karboksilik asit sentezine genel bir yaklaşım ” , J. Am. Chem. Soc. , cilt. 107, n O , 14,1985, s. 4346–4348 ( ISSN 0002-7863 ve 1520-5126 , DOI 10.1021 / ja00300a054 ).
- (inç) RA Holton , HB Kim vd. , “ Taksolün ilk toplam sentezi. 2. C ve D halkalarının tamamlanması ” , J. Am. Chem. Soc. , cilt. 116, n, o , 4,1994, s. 1599-1600 ( ISSN 0002-7863 ve 1520-5126 , DOI 10,1021 / ja00083a067 ).
- (inç) PA Wender , NC Badham ve diğerleri. , " Taksanlara giden pinen yolu. 5. Çok yönlü bir taksan öncüsünün stereo kontrollü sentezi ” , J. Am. Chem. Soc. , cilt. 119, n o 11,1997, s. 2755–2756 ( ISSN 0002-7863 ve 1520-5126 , DOI 10.1021 / ja9635387 ).
- (in) AB Dounay ve CJ Forsyth , " Okadaik asidin C3-C14 (İkame edilmiş 1,7-dioksaspiro [5.5] undec-3-ene) sisteminin kısaltılmış sentezi " , Org. Lett. , cilt. 1, n o 3,1999, s. 451–454 ( ISSN 1523-7060 ve 1523-7052 , DOI 10.1021 / ol9906615 ).
- (en) B. Malgesini , B. Forte vd. , " (-) - chaetominin'in basit bir toplam sentezi " , Chem. Avro. J. , cilt. 15, n o 32,2009, s. 7922–7929 ( ISSN 0947-6539 ve 1521-3765 , DOI 10.1002 / chem.200900793 ).
- (inç) L. Bohé G. Hanquet vd. , " Yeni bir kiral oksaziridinyum tuzunun stereospesifik sentezi " , Tetrahedron Lett. , cilt. 34, n o 45,1993, s. 7271–7274 ( ISSN 0040-4039 , DOI 10.1016 / S0040-4039 (00) 79306-3 ).
- (in) A. Arnone , S. Foletto vd. , " Aktive edilmemiş hidrokarbon sahalarının perfloro-cis-2-n-butil-3-n-propiloksaziridin ile yüksek oranda enantiyospesifik oksi-fonksiyonalizasyonu " , Org. Lett. , cilt. 1, n o 21999, s. 281–284 ( ISSN 1523-7060 ve 1523-7052 , DOI 10.1021 / ol990594e ).
- (de) E. Schmitz , R. Ohme vd. , " Isomere Oxime mit Dreiringstruktur " , Chem. Ber. , cilt. 97, n o 9,1964, s. 2521–2526 ( ISSN 0009-2940 , DOI 10.1002 / cber.19640970916 ).
- (en) S. Andeae ve E. Schmitz , " Oksaziridinlerle Elektrofilik aminasyonlar " , Sentez , n o 5,1991, s. 327-341 ( ISSN 0039-7881 ve 1437-210X , DOI 10.1055 / s-1991-26459 ).
- (en) J. Aubé , " Asimetrik sentezde oksiziridin yeniden düzenlemeleri " , Chem. Soc. Rev. , cilt. 26, n, o , 4,1997, s. 269-277 ( ISSN 0306-0012 ve 1460-4744 , DOI 10.1039 / CS9972600269 ).
- (en) A. Lattes , E. Oliveros vd. , “ Oksaziridinlerin fotokimyasal ve termal yeniden düzenlenmesi. Stereoelektronik kontrol teorisini destekleyen deneysel kanıt ” , J. Am. Chem. Soc. , cilt. 104, n o 14,1982, s. 3929-3934 ( ISSN 0002-7863 ve 1520-5126 , DOI 10,1021 / ja00378a024 ).
- “ Yohimbe, ” dan nlm.nih.gov (erişilen 27 Ağustos 2012 ) .
- ( Fr ) Bu makale kısmen veya tamamen Wikipedia makalesinden alınmıştır İngilizce başlıklı " oksaziridinle " ( yazarların listesini görmek ) .