Argon
| Argon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Katı ve sıvı argon. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pozisyon periyodik tablodaki | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Sembol | Ar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soyadı | Argon | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomik numara | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grup | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dönem | 3 E süresi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Engellemek | p'yi engelle | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| eleman ailesi | soygazlar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronik konfigürasyon | [ Ne ] 3 sn 2 3 p 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Enerji seviyesine göre elektronlar | 2, 8, 8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elementin atomik özellikleri | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| atom kütlesi | 39.948 ± 0.001 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atom yarıçapı (hesap) | ( 71 pm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| kovalent yarıçap | 106 ± 10 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waals yarıçapı | 188 öğleden sonra | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Paslanma durumu | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksit | Bilinmeyen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| iyonlaşma enerjileri | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 yeniden : 15.759610 eV | 2 e : 27.62966 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 e : 40,74 eV | 4 e : 59.81 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5 e : 75.02 eV | 6 th : 91.009 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7 e : 124.323 eV | 8 e : 143.460 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 9 e : 422.45 eV | 10 e : 478.69 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 11 e : 538.96 eV | 12 e : 618.26 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 13 e : 686.10 eV | 14 e : 755.74 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 15 e : 854.77 eV | 16 inci : 918,03 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 17 e : 4 120.8857 eV | 18 e : 4 426.2296 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| En kararlı izotoplar | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Basit vücut fiziksel özellikleri | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Olağan durum | Gaz (manyetik olmayan) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
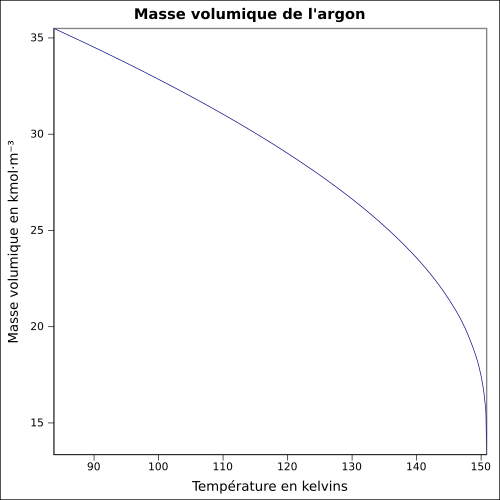
| hacimsel kütle |
1.7837 gr · L -1 ( 0 °C , 1 atm ) denklem:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| kristal sistemi | Yüz merkezli kübik | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Renk | renksiz | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| füzyon noktası | -189.36 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kaynama noktası | -185.85 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| füzyon enerjisi | 1.188 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| buharlaşma enerjisi | 6.43 kJ · mol -1 ( 1 atm , -185.85 °C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kritik sıcaklık | -122.3 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| üçlü nokta | -189.3442 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| molar hacim | 22.414 × 10 -3 m 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Buhar basıncı |
denklem:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ses hızı | 319 m · s -1 ila 20 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| kütle ısısı |
520 J · kg -1 · K -1
denklem:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termal iletkenlik | 0,01772 W · m -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Çeşitli | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| K O AKA | 100.028.315 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O EC | 231-147-0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Önlemler | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Uyarı H280 ve P403 H280 : Basınçlı gaz içerir; ısıtılırsa patlayabilir P403 : İyi havalandırılan bir yerde saklayın. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 İLE, A : Sıkıştırılmış gaz kritik sıcaklığı = -122.4 ° C Sınıflandırma kriterlerine göre % 1.0'da açıklama |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ulaşım | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20 : ikincil risk oluşturmayan boğucu gaz veya gaz UN numarası : 1006 : SIKIŞTIRILMIŞ ARGON Sınıfı: 2.2 Sınıflandırma kodu: 1A : Sıkıştırılmış gaz, aspxiant; Etiket: 2.2 : Yanıcı olmayan, toksik olmayan gazlar (A veya büyük O ile gösterilen gruplara karşılık gelir); 
22 : soğutulmuş sıvılaştırılmış gaz, boğucu UN numarası : 1951 : SOĞUTULMUŞ SIVI ARGON Sınıf: 2.2 Sınıflandırma kodu: 3A : Soğutulmuş sıvılaştırılmış gaz, boğucu; Etiket: 2.2 : Yanıcı olmayan, toksik olmayan gazlar (A veya büyük O ile gösterilen gruplara karşılık gelir);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aksi belirtilmedikçe SI ve STP birimleri . | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Argon olan kimyasal element arasında atom numarası 18 ve sembolü , Ar. Bu ait grup periyodik tablonun 18 bir parçasıdır ve ailesinin bir asil gazlar , aynı zamanda içeren, "asal gazlar" olarak adlandırılan helyum , neon , kripton , ksenon ve radon . Argon olan 3 üçüncü en bol kurucu dünya atmosferinin bir ile kütle fraksiyonu bir tekabül eden, 1.288% ve hacim bölümü 0.934% (ya da 9340 arasında ppm ) ve dünyanın. 'En bol soy gazdır Yer kabuğunun , 1.5 ppm için hesap . Dünya atmosferinde argon hemen hemen tamamen oluşur ve 40, argon , bir radyojenik nüklit elde edilen arasından çürüme ve potasyum 40 gözlenen argon ise, evrenin temel olarak oluşur ve 36, argon ile üretilen, yıldız çekirdek sentezi içinde süpernovaların .
Adı argon gelen eski Yunan , "boşta" anlamına gelen ἀργόν "tembel" Aslında atfen, [Yunanca kelime "iş olmadan" anlamına ἀεργός oluşan ἀεργός, "boşta" türetilmiştir] Bu o element kimyasal olarak inerttir. Bu elektronik konfigürasyonu bir sunulur doymuş valans tabaka stabilitesinin Kalkış ve kurma sanal imkansızlığı de kovalent bağlar . Sıcaklık ve 83,805 8 K barındırmayan üçlü nokta referans noktalarından biri olan , 1990 Uluslararası Sıcaklık Ölçeği (ITS-90).
Argon endüstriyel olarak sıvılaştırılmış havanın fraksiyonel damıtılmasıyla üretilir . Reaktif maddeler içeren yüksek sıcaklıkta kaynak ve çeşitli endüstriyel işlemler için öncelikle inert bir atmosfer olarak kullanılır . Bu nedenle , grafit elektrik ark fırınlarında , ikincisinin yanmasını önlemek için bir argon atmosferi kullanılır . Ayrıca akkor lambalar , flüoresan tüpler ve gaz tüpleri ile aydınlatmada argon kullanır . Mavi-yeşil gaz lazerleri üretmek için kullanılır .
Ana özellikler
Argon gaz, sıvı veya katı halde renksiz, kokusuz, yanıcı ve toksik değildir. Bu çözünürlük , su içinde aşağı yukarı karşılaştırılabilir oksijen ve bu 2.5 kat olduğu azot . Hemen hemen her koşulda kimyasal olarak inerttir ve oda sıcaklığında onaylanmış herhangi bir kimyasal oluşturmaz .
Ancak argon, bazı aşırı denge dışı koşullar altında kimyasal bileşikler oluşturabilir. Argon fluorohydrure harf Bu şekilde elde edilmiştir fotoliz ultraviyole arasında hidrojen florit bir matris içinde HF kriyojenik arasında iyodür sezyum CsI ve Ar argon; 27 K'nin ( -246.15 °C ) altında kararlı , kızılötesi spektroskopi ile tanımlandı . Argon fluorohydride nötr ve stabil olan bir argon sadece bilinen bir bileşiktir temel durum .
Ayrıca argon oluşturabilen klatratlar içinde su atomları tarafından oluşturulan üç boyutlu kafes içinde sıkışıp zaman buz . Ayrıca argon hidrit katyonu ArH + gibi argon içeren çok atomlu iyonlar ve Ar 2 gibi eksipleksler de vardır.* ve ArF *. Ar C ve Ar If bağlarına sahip çeşitli bileşikler, sayısal simülasyonla tahmin edilmiş ancak laboratuvarda sentezlenmemiştir.
Ana izotoplar argon mevcut yer kabuğunda olan 40 argon ( 40 % 99,6 kadar Ar), argon 36 ( 36 % 0.34 kadar, Ar) ve argon 38 ( 38 % 0.06 boyunca Ar). Potasyum-40 ( 40 K) dağılır % 11.2 oranında kendiliğinden 40, argon ile elektron yakalama veya emisyon tomografisi ve 88.8% arasında bir miktarda kalsiyum 40 ( 40 ile Ca) β parçalanma - bir ile yarı-ömrü (yarım -yaşam) 1,25 milyar yıl. Bu süre ve oluşan yan ürünler arasındaki oran, potasyum-argon tarihleme yöntemi ile kayaların yaşının belirlenmesini mümkün kılmaktadır .
Olarak dünya atmosferinin , argon 39 etkileşimi tarafından üretilir kozmik radyasyona ile argon 40 tarafından nötron yakalanması çift ardından nötron emisyon . Toprak altında, potasyum 39'dan nötron yakalama ve ardından proton emisyonu ile de üretilebilir .
Argon 37 boyunca üretilen altı testlerden gelen kalsiyum 40 , ardından nötron yakalama ile α parçalanma ; 35 günlük bir yarı ömre sahiptir.
Argon, izotopik bileşiminin Güneş Sisteminin bir bölgesinden diğerine önemli ölçüde değişmesi bakımından dikkat çekicidir . Ana kaynağı, potasyum 40'ın kayalarda radyoaktif bozunması olan argon , atmosferi tutan karasal gezegenlerde olduğu gibi esas olarak argon 40'tan oluşur : Venüs , Dünya ve Mars . Öte yandan, doğrudan oluşturması argon yıldız çekirdek sentezi esas olarak oluşur 36 argon ile üretilen alfa reaksiyon durumunda olduğu, güneş argon% 84.6 olan, argon 36 ölçümlerine göre güneş rüzgar . 36 Ar: 38 Ar: 40 Ar izotoplarının göreli bolluğunun 8400:1600:1 olduğu dev gezegenlerde de durum aynıdır .
Ek olarak, karasal bir atmosfer bir sahiptir, hacim fraksiyonu 0.934%, argon, ya da 9,340 arasında ppm , Cıva 'nın bir atmosfer 0.07 içeren ppm , Venüs'ün bu 70 içeren ppm ve Mars olduğu 19. 300 içeren ppm veya% 1.93.
Dünya atmosferindeki radyojenik argon 40'ın baskınlığı , Dünya'nın argonunun atom kütlesinin , 39.95 u mertebesinde , potasyumunkinden 0.85 u daha büyük olmasından sorumludur , bu da onu elementlerin periyodik tablosunda takip eder ve atom kütlesi 39.10 u mertebesinde olan . Bunun nedeni 1894 yılında argon keşfinden sırasında paradoksal görünüyordu Dmitri Mendeleïev potasyum arasındaki yeri argon zorunda yol açtı atom kütlesini, artan sırayla onun periyodik tablo düzenlenmiş vardı kalsiyum etrafında 40 bir atom kütlesi ile, 08 u ve karıştırılmaması bu 0.13 olan argon u 3.65 atomik kütle farkı yoktu iken, u arasında klor (35.45 u ) ve potasyum (39.10 u ). Bu problem, 1913'te periyodik tablonun elementleri doğru sıraya koyan artan atom kütlesine göre değil artan atom numarasına göre düzenlenmesi gerektiğini gösteren Henry Moseley tarafından çözüldü .
Atmosferik bolluk diğerine göre nispi argon soy gazlar - 9340 ppm , argon, 5.24 karşı ppm arasında helyum , 18.18 ppm arasında neon , 1.14 ppm arasında kripton ve 0.087 ppm arasında iksenon - de atfedilebilir radyojenık argon 40 : 36 Argon gerçekten var sadece 31.5 ppm'lik bir bolluk ( 9340 ppm'nin %0.337'si ), neon (18.18 ppm ) ile aynı büyüklük mertebesinde .
Bileşikler
Argon atomu , bir yer alır elektron doymuş değerlikli kabuk ile, tam s ve s alt katmanlar . Bu, bu elementi kimyasal olarak inert ve çok kararlı yapar, yani diğer atomlarla ancak çok zor bir kimyasal bağ oluşturur . Kadar 1962 , asal gazlar oluşumu için tamamen nötr ve uygun olduğu kabul edilmiştir kimyasal bileşikler ; ancak bu tarihte, ksenon heksafloroplatinat XePtF 6'nın sentezi soy gazların kimyasının yolunu açmıştır .
W (CO) 5 Ar kimyasal formülüne sahip tungsten pentakarbonil ile argonun ilk bileşiği, 1975'te yayınlandı, ancak gerçek varlığı tartışmalıdır. 1962 yılında sentezlenmiştir Helsinki Üniversitesi , argon fluorohydride tarafından Harf fotoliz ultraviyole arasında hidrojen florit bir matris içinde HF kriyojenik arasında sezyum iyodür altında kararlı bir bileşik, argon CSI ve Ar 27 K ( -246,15 ° C ) ile tanımlanır kızılötesi spektroskopi . Bu keşif, argonun zayıf bağlı bileşikler oluşturabileceği fikrine yol açtı.
Dikatyondur yarı kararlı ARCf 22+ , karbonil florür COF 2 ile izoelektronikve fosgen COCI 2valans elektronları açısından bakıldığında , 2009 yılında bir karbon – argon bağı uygulanarak gözlenmiştir . Moleküler iyon 36 ArH + , tekabül eden , argon hidrit katyon 36 (argonium) tespit edilmiştir yıldızlararası ortamın seviyesinde Yengeç Nebula ; uzayda tespit edilen ilk soy gaz bileşiğidir .
Katı argon hidrit Ar (H 2 ) 2a, Waals der Van bileşiği aynı olan bir kristal yapısı olarak Laves faz (tr) MgZn 2. Bu arasındaki basınçlarda meydana 4.3 ve 220 GPa ile elde edilen sonuçlar da, Raman spektroskopisi göstermektedir ki, H 2 molekülleriAr (H 2 ) 2 bileşiğinin175 GPa'nın üzerinde ayrışır .
Endüstriyel üretim ve uygulamalar
Argon ile endüstriyel olarak üretilmektedir fraksiyonel damıtma arasında sıvılaştırılmış hava birimlerinde kriyojenik bir hava damıtma (in) , ayırmak için bir yöntem , sıvı azot kaynadığı, 77.3 K kaynar, argon 87.3 K ve sıvı oksijen de kaynar 90.2 K . Dünya argon üretimi yılda 700.000 ton civarındadır.
Argon, endüstriyel kullanımını haklı çıkaran birkaç ilginç özelliğe sahiptir:
- kimyasal olarak inert bir gazdır;
- nitrojen yeterince inert olmadığında ucuz bir alternatiftir ;
- düşük ısı iletkenliğine sahiptir (bu nedenle bir ısı yalıtkanıdır );
- elektronik özellikleri ( iyonizasyon , emisyon spektrumu ) belirli aydınlatma uygulamalarında kullanılmaktadır.
Diğer soygazlar benzer özellikleri sergileyen ve iyi olarak kullanılabilir, ancak argon ekstre bir yan ürün olarak elde edilen, çok bütün ucuz olan oksijen ve azot arasından hava kriyojenik fraksiyonel damıtma ile.
Endüstriyel uygulamalar
Argon, kimyasal olarak inert maddelerin reaktif hale gelme eğiliminde olduğu bazı yüksek sıcaklıktaki endüstriyel işlemlerde kullanılır. Bir argon atmosferi böylece kullanılan elektrikli fırınlar ile grafit elektrotlar olarak önlemek için yanma , bu malzeme elde edildi.
Bu işlemlerin bazıları için, nitrojen veya oksijenin varlığı malzemede kusurlara neden olur. Argon, gaz metal ark kaynağı ve TIG kaynağı gibi belirli ark kaynağı türlerinin yanı sıra titanyum ve diğer element reaktiflerinin tedavisinde kullanılır . Yarı iletken endüstrisine yönelik silikon ve germanyum kristalleri de kristal kalitelerini sağlamak için argon atmosferinde yetiştirilir .
Argon için bir yöntem olarak kümes hayvanları endüstrisinde kullanılan atıl gaz ile boğularak için oksijensiz kümes bir hastalığın başlangıcından sonra bir kütle kesimi ya da alternatif kesim için bir araç olarak ya da, electronarcosis . Argonun havaya göreli yoğunluğu, gaz verirken zemine yakın kalmasına neden olur. Reaktif olmaması onu gıda ürünleri ile uyumlu kılar ve dokularda kısmen oksijenin yerini alması gıdaların raf ömrünü uzatır.
Argon bazen bilgisayar sunucuları gibi su veya köpük kullanımından zarar görebilecek değerli ekipmanları koruyarak yangınları söndürmek için kullanılır.
Tıbbi uygulamalar
Usulleri kriyoterapi (in) gibi kriyoablasyona (in) yok etmek için, sıvı argon kullanımı dokuları gibi , kanser hücreleri . Adı verilen bir prosedür kullanmak mümkün olmuştur argon koagülasyona bir biçimidir, elektro (in) ile plazma meşale olan bir risk oluşturmaktadır, ancak gaz embolisi , en az bir hastanın ölümüyle gerçekleşmiştir.
Argon mavi lazerler kullanılır ameliyatı için dikiş arterler , tahrip tümörleri içinde göz ameliyatı veya buraya elektrokoagülasyon vasıtasıyla endoskopik yetkililerin lezyonlar gastrointestinal kanama.
Ayrıca argon yerine test edilmiştir azot içinde solunum gazı denir Argox içinde çözünmüş azot çıkarılmasını hızlandırmak için , kan .
Bilimsel araştırma
Sıvı argon, nötrino tespiti ve karanlık madde araştırmaları için bir hedef olarak kullanılır . Varsayımsal arasındaki etkileşimler wimps ve çekirdek arasında , argon atomları bir üretmelidir gözlemlenebilir sintilasyon ile foto-çoğaltıcı tüpler . Argon gazı içeren iki fazlı dedektörler, WIMP-argon çekirdeği etkileşimleri sırasında iyonizasyon tarafından üretilen elektronları tespit etmek için kullanılır .
Diğer sıvılaştırılmış soy gazlar gibi, sıvı argon da yüksek bir parıldama hızına sahiptir (yaklaşık 51 foton / keV ), kendi parıldamasına karşı şeffaftır ve arıtılması nispeten kolaydır. Ksenondan daha ucuzdur ve elektronik etkileşimleri nükleer etkileşimlerden ayırt etmeyi mümkün kılan farklı bir sintilasyon zaman profiline sahiptir. Bununla birlikte , 39 Ar'da tükenmiş , yarı ömrü sadece 269 yıl olan ve stoku 40 Ar ( n , 2 n ) 39 tarafından yeniden oluşturulmamış olan bodrum katından argon kullanılması dışında , argon tarafından kontaminasyondan dolayı daha güçlü bir radyoaktiviteye sahiptir.39 Ar, bir etkileşim bölgesinin kozmik radyasyona ile atmosfer , argon .
Başka kayıt olarak, 39 Argon tarih özellikle kullanılmış olan yeraltı ve buz çekirdekleri içinde Antarktika . K-Ar kalma ve argon argon partner ayrıca kullanılan radyometrik bir tortul , metamorfik ve volkanik .
Tutucu
Argon, sayı E938 , bir şekilde kullanılan gıda koruyucu kaldırmak için oksijen ve nem paketleme atmosferden ve son kullanma tarihini geciktirmek. Hava ile oksidasyon , hidroliz ve ürünü bozan diğer reaksiyonlar böylece geciktirilir veya tamamen bloke edilir. Kimyasal reaktifler ve farmasötik moleküller bazen bir argon atmosferinde paketlenir. Bu soy gaz aynı zamanda vernikler , poliüretan ve hatta boyalar için koruyucu olarak da kullanılır .
Argon, şarabı oksijenden korumak ve oksidasyonunu ve ayrıca istenmeyen bakteri etkileşimlerini (özellikle asetik asit üreten ve şarabı sirke dönüştüren asetik bakterileri) önlemek için şarap yapımında da kullanılır . Spreyler için itici olarak da kullanılabilir .
Laboratuvar ekipmanları
Argon, bir vakum hattına ve torpido gözüne inert gaz olarak kullanılabilir ; daha az pahalı olan nitrojene tercih edilir , çünkü nitrojen özellikle reaktif bileşiklerle ve ayrıca belirli ekipmanlarla reaksiyona girebilir. Ayrıca argon, nitrojenin aksine havadan daha yoğun olma avantajına sahiptir ve bu da pratikte kullanımını kolaylaştırır.
Argon, gaz kromatografisinde ve elektrosprey iyonizasyonunda taşıyıcı gaz olarak kullanılabilir . Endüktif olarak eşleştirilmiş plazma spektrometrisinde kullanılan plazma için tercih edilen gazdır . Argon tercihen kullanılan püskürtmeli çökeltme (In) numuneler üzerinde tarafından incelenecek Taramalı Elektron Mikroskobu ve temizlenmesi için gofret içinde mikroimalat .
Aydınlatma
Bir akkor lamba genellikle korumak için argon ile doldurulmuştur filament gelen yüksek sıcaklıkta oksidasyonu . Ayrıca argon tarafından radyasyonu için kullanılan iyonizasyon olarak, plazma lambaları ve kalorimetre içinde parçacık fiziği . Deşarj lambaları küçük ekleyerek mavi haline saf argon üretmek hafif uçuk mor çekme leBleu'nın lavanta, dolu cıva .
Argon, mavi ve yeşil iyon lazerleri (in) için de kullanılır .
Çeşitli uygulamalar
Argon, çift cam için ısı yalıtkanı olarak kullanılır . Kimyasal inertliği ve düşük ısı iletkenliği nedeniyle tüplü dalış için kuru giysilerin doldurulmasında da kullanılır .
Argon, uzay bilimlerinde VASIMR'ler için itici gaz olarak kullanılabilecek gazlardan biridir . Hava silahları alanında, AIM-9 Sidewinder füzeleri de dahil olmak üzere bazı havadan havaya füzelerin kafalarını gevşeterek basınç altında soğutmak için kullanılır .
Argon, atletizmde hipoksiyi simüle eden bir katkı maddesi olarak kullanılmıştır . Bu nedenle, 2020'de geri çekilmeden önce, 2014 yılında Dünya Anti-Doping Ajansı tarafından yasaklanan yöntemler ve maddeler listesine xenon ile birlikte dahil edildi .
Tarih ve etimoloji
Kelime Argon Eski Yunan türetilmiştir ἀργός / Argos ( "boşta", "tembel", "steril") özel Yunan önek a ve kelime oluşturduğu, ἔργον / ergon ( "iş"), bu etimoloji çağrıştıran atıl karakter 'öğesinden.
Kimyasal inert gaz havada varlığı ile şüphelenilen olarak Henry Cavendish erken 1785 ama ederek keşif Rab Rayleigh ve Sir William Ramsay at University College London'dan kadar bekledi 1894 . Bunu, temiz hava örneğinden oksijen , karbon dioksit , su buharı ve nitrojeni çıkararak ve argon adını verdikleri soy gaz bırakarak yaptılar . Bu iki bilim adamı , keşiflerinin resmi iletişimini Royal Society'ye yaptılar.31 Ocak 1895.
Kimyasal olarak üretilen nitrojenin, o sırada bilinen diğer atmosferik gazları uzaklaştırarak havadan çıkarılan nitrojenden %0,5 daha hafif olduğu gerçeğiyle yola koyuldular. Fraksiyonel damıtma sıvılaştırılmış hava bunları argon önemli miktarda üretmek için izin 1898 ve diğer iki izole etmek için, aynı zamanda asil gazlar , neon ve ksenon .
Ayrıca argon gözlenmiştir 1882 belirtildiği HF Newall ve WN Hartley, bağımsız çalışması sırasında spektral çizgiler içinde emisyon spektrumunda hava birisine tekabül etmeyen bilinen kimyasal element .
Argonun kimyasal sembolü 1957 yılına kadar A idi ve o zaman Ar oldu.
tehlikeler
Gibi helyum , argon düşük konsantrasyonlarda tehlikeli değildir. Bununla birlikte,% 38 daha yoğun daha hava ve teneffüs argon büyük miktarda riski taşır boğulma oksijensizlik (dan anoksi ); bu, örneğin kapalı bir alanda kaynak işlemleri sırasında meydana gelebilir .
Notlar ve referanslar
- (içinde) Beatriz Cordero Verónica Gómez, Ana E. Platero-Prats, Marc Revés Jorge Echeverría, Eduard Cremades, Flavia ve Santiago Barragan Alvarez , " Covalent radii revisited " , Dalton Transactions ,2008, s. 2832 - 2838 ( DOI 10.1039 / b801115j )
- (içinde) David R. Lide, CRC Kimya ve Fizik El Kitabı , TF-CRC,2006, 87 inci baskı. ( ISBN 0849304873 ) , s. 10-202
- (tr) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 inci baskı. , 2804 s. , Ciltli ( ISBN 978-1-420-09084-0 )
- (tr) Robert H. Perry ve Donald W. Green , Perry's Chemical Engineers' Handbook , ABD, McGraw-Hill,1997, 7 inci baskı. , 2400 s. ( ISBN 0-07-049841-5 ) , s. 2-50
- Ağırlık ve Ölçüler Uluslararası Komitesi'nin Dakika , 78 inci Oturumu, 1989, s. T1-T21 (ve s. T23-T42, İngilizce versiyonu).
- Kimyasal Özetler veritabanı SciFinder Web üzerinden sorgulandı 15 Aralık 2009 (arama sonuçları )
- IFA'nın (iş sağlığı ve güvenliğinden sorumlu Alman kuruluşu) GESTIS kimyasal veritabanındaki "7440-37-1" CAS numarasının girişi ( Almanca , İngilizce ), 30 Ocak 2009'da erişildi (JavaScript gerekli)
- " Argon kimyasal ürünlerin veritabanındaki" Reptox ait CSST 25 Nisan 2009 erişilen (iş güvenliği ve sağlığı sorumlu Quebec örgütü),
- (in) Markku Räsänen , " Havadan Argon " , Nature Chemistry , cilt. 6, n o 1, Ocak 2014, Madde n o 82 ( PMID 24345939 , DOI 10.1038 / nchem.1825 , online okuyun )
- (tr) Leonid Khriachtchev, Mika Pettersson, Nino Runeberg, Jan Lundell ve Markku Räsänen , “ Kararlı bir argon bileşiği ” , Nature , cilt. 406, n o 6798, 24 Ağu 2000, s. 874-876 ( PMID 10972285 , DOI 10.1038 / 35022551 , Bibcode 2000Natur.406..874K , çevrimiçi okuyun )
- (in) VR Belosludov OS Subbotin DS Krupskii, Prokuda OV, RV ve Y. Belosludov Kawazoe , " Mikroskobik klatrat bileşikleri modeli " , Journal of Physics: Conference Series , Cilt. 29, n o 1, ocak 2006, s. 1-7 ( DOI 10.1088 / 1742-6596 / 29/1/001 , Bibcode 2006JPhCS..29 .... 1B , çevrimiçi okuyun )
- (içinde) Arik Cohen, Jan Lundell ve R. Benny Gerber , " Argon-argon ve karbon-silikon kimyasal bağları olan ilk bileşikler " , Journal of Chemical Physics , cilt. 119, n o 13, Ekim 2003, s. 6415-6417 ( DOI 10.1063/1.1613631 , Bibcode 2003JChPh.119.6415C , çevrimiçi okuyun )
- (tr) J. Emsley, Nature's Building Blocks , Oxford University Press, 2001, s. 44-45 . ( ISBN 978-0-19-960563-7 )
- Étienne Roth ( yön. ), Bernard Poty ( yön. ), Robert Delmas et al. ( pref. Jean Coulomb ), Doğal nükleer fenomenlerle tarihleme yöntemleri , Paris, Éditions Masson , coll. " CEA Koleksiyonu ",1985, 631 s. ( ISBN 978-2-225-80674-2 , bildirim BNF n O FRBNF34836710 ) , Chap. 17 ("Silikon 32 ve argon 39")
- (içinde) Yeraltı Nükleer Patlamalarının İzleyicisi Olarak 37 Ar için Bilim Örneği , sayfa 1, 2010
- (içinde) Katharina Lodders , " Solar Bolluk Argon " , The Astrophysical Journal , cilt. 674, n, o , 1, 10 Şubat 2008, s. 607-611 ( DOI 10,1086 / 524.725 , bibcode 2008ApJ ... 674..607L , arXiv arXiv: 0.710,4523 , çevrimiçi okuma )
- (içinde) AGW Cameron , " Dış gezegenlerdeki uçucu Elementlerin elemental ve izotopik bollukları " , Space Science Reviews , cilt. 14, n kemik 3-4, Mart 1973, s. 392-400 ( DOI 10.1007 / BF00214750 , Bibcode 1973SSRv ... 14..392C , çevrimiçi okuyun )
- (içinde) Marco Fontani , Mariagrazia Costa ve Mary Virginia Orna , Kayıp Elementler: Periyodik Tablonun Gölge Tarafı , New York, Oxford University Press ,2015( 1 st ed. 2014), 531 , s. ( ISBN 9780199383344 ) , s. 182.
- (inç) Neil Bartlett , " Ksenon heksafloroplatinat Xe + [PtF 6 ] - " , Proceedings of the Chemical Society , n o 6,Haziran 1962, s. 197-236 ( DOI 10.1039 / PS9620000197 , çevrimiçi okuyun )
- (içinde) Nigel A. Young , " Düşük sıcaklıkta ana grup koordinasyon kimyası: Matrisle izole edilmiş Grup 12 ila Grup 18 komplekslerinin bir incelemesi " , Koordinasyon Kimyası İncelemeleri , cilt. 257 n kemik 5-6, Mart 2013, s. 956-1010 ( DOI 10.1016 / j.ccr.2012.10.013 , çevrimiçi okuyun )
- (içinde) Neil Bartlett , " The Noble Gases " , Chemical & Engineering News , Cilt. 81, n o 36, 8 Eylül 2003, s. 32-34 ( DOI 10.1021 / cen-v081n036.p032 , çevrimiçi okuyun )
- (in) Jessica F. Lockyear Kevin Douglas Stephen D. Fiyat, Małgorzata karwowska Karol J. Fijalkowski Wojciech Grochala Marek remes Jana Roithová Detlef Schroeder , " ARCf Üretimi 2 2+ Dication ”, The Journal of Physical Chemistry Letters ,cilt. 1,n o 1,8 Aralık 2009, s. 358-362 ( DOI 10.1021 / jz900274p , çevrimiçi okuyun )
- (tr) J. Barlow, BM Swinyard, PJ Owen, J. Cernicharo, HL Gomez, RJ Ivison, O. Krause, TL Lim, M. Matsuura, S. Miller, G. Olofsson ve AND Polehampton , " Detection of a Soy Gaz Moleküler İyon, 36 ArH + , Yengeç Bulutsusu'nda ” , Science , cilt. 342, n O , 6164, 13 Aralık 2013, s. 1343-1345 ( PMID 24337290 , DOI 10.1126 / science.1243582 , Bibcode 2013Sci ... 342.1343B , çevrimiçi okuyun )
- (in) Annette K. Kleppe, Mónica Amboage ve Andrew P. Jephcoat , " Yeni yüksek basınçlı van der Waals bileşiği Kr (H 2) 4 kripton-hidrojen ikili sisteminde keşfedildi ” , Scientific Reports , cilt. 4,16 Mayıs 2014, Makale n o 4989 ( DOI 10.1038 / srep04989 , bibcode 2014NatSR ... 4E4989K , çevrimiçi okuma )
- " Elementlerin Periyodik Tablosu: Argon - Ar " , Environmentalchemistry.com ( 12 Eylül 2008'de erişildi )
- (içinde) Sara J. Shields ve ABM Raj , " Kümes Hayvanları Kesimi için Elektrikli Su Banyosu Sersemletme Sistemlerinin Eleştirel İncelemesi ve Alternatif Teknolojilerdeki Son Gelişmeler " , Journal of Applied Animal Welfare Science , cilt. 13, n o 4, 2012, s. 281-299 ( PMID 20865613 , DOI 10.1080 / 10888705.2010.507119 , çevrimiçi okuyun )
- DL Fletcher , " Slaughter Technology, " Sempozyum: Kanatlı Kesim Teknolojisinde Son Gelişmeler ,1999( Oku Online , erişilen 1 st Ocak 2010 )
- (içinde) MJ Fraqueza ve AS Barreto , " Etki, argon karışımı ile değiştirilmiş atmosferli paketlemenin hindi eti raf ömrüdür " , Poultry Science , cilt. 88, n o 9, Eylül 1999, s. 1991-1998 ( PMID 19687286 , DOI 10.3382 / ps.2008-00239 , çevrimiçi okuyun )
- (içinde) Joseph Z. Su, Andrew K. Kim, George P. Crampton ve Zhigang Liu , " İnert Gaz Ajanları ile Yangın Söndürme " , Yangından Korunma Mühendisliği Dergisi , cilt. 11, n o 2 2001, s. 72-87 ( DOI 10.1106 / X21V-YQKU-PMKP-XGTP , çevrimiçi okuyun )
- (in) " Argon Gelişmiş Pıhtılaşmanın Laparoskopik Kullanımı Sırasında Aşırı Basıncın Neden Olduğu Ölümcül Gaz Embolisi " , Health Devices , cilt. 23, n o 6, Haziran 1994, s. 257-259 ( çevrimiçi okuyun )
- (içinde) Jerome Canady , Kimberly Wiley ve Biagio Ravo , " argon plazma pıhtılaşması ve endoskopik problar için gelecekteki uygulamalar İkili Mod " , Gastroenterolojik Bozukluklarda İncelemeler , Cilt. 6, n o 1,2006, s. 1-12 ( ISSN 1533-001X , PMID 16520707 , çevrimiçi okuma , erişim tarihi 9 Ekim 2017 ).
- (içinde) Andrew A Pilmanis Ulf I. Balldin, James T. Webb ve Kevin M. Krause , " %100 Argon-Oksijen ve Oksijen Solunumu Kullanarak 3.5 Psi'ye Kademe Dekompresyon " , Havacılık, Uzay ve Çevre Tıbbı , uçuş . 74, n o 12, aralık 2003, s. 1243-1250 ( PMID 14692466 , çevrimiçi okuyun )
- (in) , Dan Gastler Ed Kearns, Andrew Hime, Laura C. Stonehill stan Seibert Josh Klein Hugh W. Lippincott Daniel N. McKinsey ve James A. Nikkel , " sıvı argon nükleer geri teper sintilasyon verimliliği Ölçümü ” , Fiziksel İnceleme C , cilt. 85, n o 6, 27 Haziran 2012, Eşya , n O 065.811 ( DOI 10,1103 / PhysRevC.85.065811 , bibcode 2012PhRvC..85f5811G , arXiv 1004,0373 , online okuyun )
- (in) J.Xu F. Calaprice, C. Galbiati, A. Goretti Guray G., T. Hohman, D. Holtz, An. Ianni, Bay Laubenstein, Loer B., C. Lovec, CJ Martov , D Montanari, S. Mukhopadhyay, A. Nelson, SD Rountree, RB Vogelaar ve A. Wright , “ Derin yeraltı kaynaklarından argonda iz 39 Ar içeriğinin incelenmesi ” , Astroparticle Physics , cilt. 66, haziran 2015, s. 53-60 ( DOI 10.1016 / j.astropartphys.2015.01.002 , bibcode 2015APh .... 66 ... 53X , arXiv 1204,6011 , çevrimiçi okuma )
- Paul Depovere, Elementlerin Periyodik Tablosu . Evrenin temel harikası , De Boeck Supérieur ,2002, s. 98.
- (tr) Henry Cavendish , " XXIII. Havada deneyler. ” , Londra Kraliyet Cemiyetinin Felsefi İşlemleri , cilt. 75, 1785, s. 372-384 ( DOI 10.1098 / rstl.1785.0023 , Bibcode 1785RSPT ... 75..372C , çevrimiçi okuyun )
- (içinde) Robert John Strutt ve William Ramsay , " I. Argon, atmosferin yeni bir biçimi " , Londra Kraliyet Cemiyeti Bildirileri , cilt. 57, 1895, s. 265-287 ( DOI 10,1098 / rspl.1894.0149 , Özyeğin 115394 , çevrimiçi okuma )
- (içinde) John William Strutt ve William Ramsay , " VI. Atmosferin yeni bir bileşeni olan Argon ” , Londra Kraliyet Cemiyeti'nin Felsefi İşlemleri , 1895, s. 187-241 ( DOI 10.1098 / rsta.1895.0006 , JSTOR 90645 , Bibcode 1895RSPTA.186..187R , çevrimiçi okuyun )
- (in) Sir William Ramsay, " Atmosferin Nadir Gazları " , https://www.nobelprize.org/'da , Nobel Kimya Ödülü , 12 Aralık 1904( 14 Haziran 2020'de erişildi ) .
- (içinde) John H. Holloway, soy gaz kimyası , Methuen,1968, s. 6
- (içinde) John Emsley, Nature's Building Blocks: An AZ Guide to the Elements , Oxford University Press, 2003, s. 36 . ( ISBN 0198503407 )
- (in) Norman E. Holden, " Kimyasal Elementlerin Kökeni ve Keşfedicilerinin Tarihi ' , Brisbane, Avustralya'daki 41. IUPAC Genel Kurulu 29 Haziran - 8 Temmuz 2001 , https: //www.nndc.bnl. gov / , Ulusal Nükleer Veri Merkezi , 12 Mart 2004( 14 Haziran 2020'de erişildi ) .
Şuna da bakın:
İlgili Makaleler
Dış bağlantılar
- (tr) “ Argon Teknik veriler ” (erişilen 2016 24 Nisan ) alt sayfalarda her izotop için bilinen verilerle,
- (In) Argonun farklı formlardaki görüntüleri
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | Hey | |||||||||||||||||||||||||||||||
| 2 | Li | olmak | B | VS | OLUMSUZLUK | Ö | F | Doğmak | |||||||||||||||||||||||||
| 3 | Yok | Mg | Al | Evet | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | o | sc | Ti | V | cr | Mn | Fe | ortak | Veya | Cu | çinko | ga | Ge | As | Gör | Br | Kr | |||||||||||||||
| 5 | Rb | Bay | Y | Zr | not | ay | Tc | Ru | Rh | PD | Ag | CD | İçinde | Sn | Sb | Sen | ben | Xe | |||||||||||||||
| 6 | C'ler | Ba | NS | Bu | Halkla İlişkiler | Nd | Öğleden sonra | Sm | NS | gd | yemek | dy | Ho | Er | Tm | yb | Okumak | hf | Senin | W | NS | Kemik | ir | nokta | NS | Hg | TL | Pb | Bi | po | NS | Rn | |
| 7 | Cum | Ra | AC | NS | baba | sen | np | NS | NS | Santimetre | bk | bkz. | Dır-dir | FM | md | Numara | lr | Rf | db | Çavuş | bh | hs | dağ | Ds | Rg | Müşteri | Nh | fl | Mc | Sv. | Ts | og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
|
Alkali Metaller |
alkali toprak |
Lantanitler |
geçiş metalleri |
Zayıf metaller |
metal- loidler |
Olmayan metaller |
halo genleri |
soy gazlar |
Sınıflandırılmamış öğeler |
| aktinitler | |||||||||
| süperaktinitler | |||||||||